Varón joven con neoplasia linfoide
Presentación de caso clínico en ateneo de la SAH por FUNDALEU.
Young man with lymphoid malignancy
Pavlovsky A., Mela Osorio MJ., Narbaitz M., García Montenegro M., Galeano A., Pavlovsky MA.
FUNDALEU, J. E. Uriburu 1450, (1114) Buenos Aires, Argentina.
E-mail: astridp@intramed.net
Palabras claves: LNH-T anaplásico ALK negativo,
diagnóstico,
tratamiento,
recaída,
brentuximab vedotin.
Key words: anaplasic large cell lymphoma,
diagnosis,
treatment,
relapse,
brentuximab vedotin.
Resumen
Se describe el caso de un paciente joven con linfoma no Hodgkin T (LNH- T) y su manejo en la vida real. Se describen pasos diagnósticos y se discute bibliografía para definir tratamiento de primera línea y en recaída.
Abstract
We present a case of a young patient with anaplastic large cell lymphoma ALK negative. We describe the importance of a precise diagnosis and challenges in first line and in relapse setting.
Paciente de sexo masculino de 37 años de edad, derivado por Clínica Médica por poliadenopatías palpables y diagnóstico presuntivo de enfermedad linfoproliferativa.
Al momento de la primera entrevista relataba cuadro de pérdida de peso de 8 Kg en los últimos 3 meses, sudoración nocturna y astenia marcada que comenzaba a limitar sus actividades diarias.
La tomografía solicitada por médico de cabecera informaba adenomegalia submandibular izquierda de 30 x 22 mm, cervical izquierda de 20 mm, mediastinal de 40 mm x 22 mm y un conglomerado retroperitoneal. Se había realizado una biopsia de ganglio cervical cuya histología informaba: linfoma de alto grado de agresividad histológica vinculable a linfoma de células grandes anaplásico ALK negativo (OMS). Con estos hallazgos fue derivado a nuestra institución en mayo del 2015.
Al examen físico inicial se evidenciaba la pérdida de peso y presentaba adenomegalias cervicales e inguinales bilaterales. Sin organomegalias palpables.
En el laboratorio se constataba anemia leve, el resto del hemograma era normal como así también la LDH y el resto de la química. Las serologías virales fueron negativas (Tabla 1).
Tabla 1. Laboratorio al ingreso
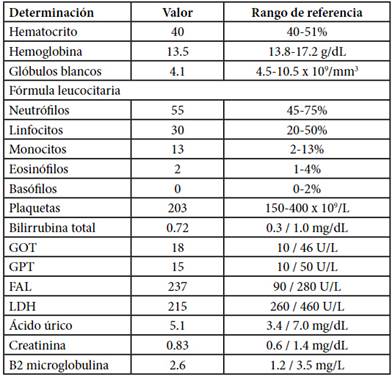
El paciente presentaba antecedentes de cirugía de by-pass gástrico 3 años atrás (2012) y tabaquismo severo (25 paquetes por año).
1) Diagnóstico y estratificación de riesgo
En nuestra institución se realizó revisión del taco de biopsia de ganglio y biopsia de médula ósea para confirmar el diagnóstico. El medulograma mostraba celularidad normal sin evidencia de infiltración por enfermedad linfoproliferativa. La citometría de flujo y patología de la médula ósea confirmaban ausencia de infiltración.
Se completó estadificación con PET-TC. El estudio mostró imágenes de concentración patológica del radiotrazador en múltiples adenopatías hipermetabólicas y en focos hipermetabólicos óseos, que interpretamos como vinculados a compromiso nodal y extra nodal de enfermedad linfoproliferativa (Figura 1).
Figura 1. Hallazgos del PET-TC al diagnóstico
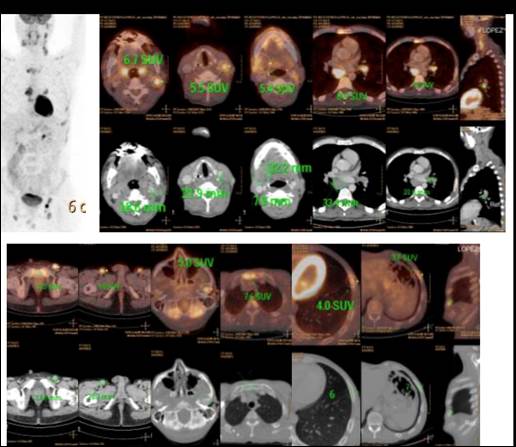
- El paciente presentaba estadio de Ann Arbor: IV B
- Índice Pronóstico Internacional (IPI): 2
- Índice Pronóstico en Linfoma T (PIT): 0.
2) Tratamiento de primera línea
Tratamiento de primera línea
Inducción con CHOP x 6 ciclos realizado ambulatorio en hospital de día con buena tolerancia y sin intercurrencias relevantes.
La evaluación de respuesta a la inducción con PET evidenció remisión completa metabólica (RCm).
Tratamiento de consolidación
Se procedió a tratamiento de consolidación con altas dosis de quimioterapia y rescate con células progenitoras hematopoyéticas (noviembre 2015).
Procedimiento bien tolerado. Alta precoz.
Re-estatificación con PET post consolidación (+160): RCm sostenida.
3) Discusión del caso: LNH-T diagnósticos complicados
Los LNH-T conllevan un gran desafío al diagnóstico y al tratamiento. Teniendo en cuenta esta dificultad diagnóstica, en el 2014 se publicó una revisión de 131 casos de LNH-T cuyos diagnósticos habían sido revisados por un grupo de expertos en centros de referencia del National Comprehensive Cancer Network. La concordancia diagnóstica fue de 44%. El índice de discordancia entre los LNH-T periféricos NOS, AILTL, LNH-T anaplásico ALK – y LNH-T anaplásico ALK+ fue de 19%, 33%, 35% y 19% respectivamente.
Los autores concluyen que debido a la complejidad anatomo-patológica y molecular, los pacientes se benefician de una revisión de los preparados del diagnóstico, realizada por expertos(1).
Esta diferencia al diagnóstico es relevante ya que los diferentes subgrupos representan sobrevidas globales diferentes y, en algunos casos, una modificación en el tratamiento(2).
Estudios aún más
recientes evidencian la diferencia de expresión génica entre los diferentes
subtipos histológicos y, nuevamente, una discordancia notable entre el
diagnóstico realizado por inmunohistoquímica y aquél definido por su perfil
molecular (Figura 2)(3)![]() .
.
Figura 2. Discordancia entre el diagnóstico realizado por inmunohistoquímica y el definido por perfil molecular
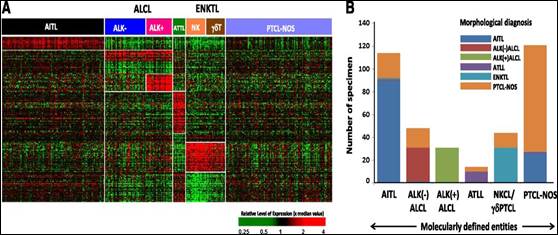
A pesar de estos avances en el entendimiento de los LNH-T, no se ha observado un impacto en la mejoría en las opciones terapéuticas, y los tratamientos actuales se asocian a un alto índice de refractariedad o recaída con una sobrevida global (SG) a 5 años de 35% sin diferencias significativas con aquélla reportada hace una década.
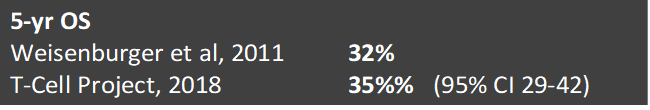
EL IPI representa una evaluación pronóstica útil en estos pacientes, pero, al igual que en otros linfomas, en LNH-T se han desarrollado varios índices pronósticos específicos que incluyen características de los pacientes, de los síntomas en la presentación, de cambios de laboratorio y de la extensión de la enfermedad(4).
Ante la presentación de un paciente en consultorio con este diagnóstico hay hechos y preguntas reales que deben surgir.
Hechos:
• Se requiere siempre de tratamiento sistémico.
• Los esquemas basados en adriamicina son los más frecuentemente utilizados en primera línea...
• ...pero las recaídas tempranas son frecuentes y la SG a 5 años de aproximadamente 30%.
Y de estos hechos surgen los siguientes interrogantes:
• ¿Hay algo mejor que el CHOP para este paciente?
• ¿Es beneficioso que consolide con altas dosis de quimioterapia y rescate de células progenitoras en 1ra. línea?
Con respecto a si hay otro esquema de primera línea que ofrezca mayores beneficios que el CHOP, los datos publicados no son contundentes.
Los esquemas de quimioterapia basados en antraciclinas son, hoy en día, el tratamiento estándar en LNH-T, pero sus beneficios son cuestionados. En el 2011 un grupo de investigadores realizó una revisión sistemática de la literatura y un metaanálisis evaluando el índice de RC y SG en LNH-T periférico (LNHTP).
El índice de RC en este grupo de pacientes varía desde 35.9% (95% CI 23.4–50.7%) para LNH-T con enteropatía (ETTL) a 65.8% (95% CI 54.0–75.9%) para LNH-T anaplásico a células grandes (ALCL). La SG fue de 38.5% (95% CI 35.5–41.6%) para todo el grupo de pacientes y osciló entre 20.3% (95% CI 12.5–31.2%) para ETTL a 56.5% (95% CI 42.8–69.2%) para los ALCL.
Esta información sugiere una gran heterogeneidad en el beneficio de las antraciclinas entre los subtipos histológicos de LNH-T. Las antraciclinas logran RC en aproximadamente el 50% de los pacientes con LNHTP, logrando una SG a 5 años aceptable para pacientes con ALCL, pero no para LNHTP-NOS o ETTL(5).
Por otro lado, un estudio retrospectivo del grupo alemán observó que el grupo de pacientes menores de 60 años y con LDH dentro de los parámetros normales que utilizaron EPOCH como tratamiento de primera línea, obtuvo sobrevida libre de progresión (SLP) significativamente mejor que aquélla con el grupo de iguales características tratados con CHOP-14(6).
En una cohorte prospectiva de LNHTP que incluyó 499 pacientes, 41.8% recibieron esquemas de primera línea con adriamicina, 20.9% con adriamicina y etopósido, 15.8% con otros esquemas que incluían etopósido, (CHOEP) 2.1% con esquemas basados en gemcitabina y 19.2% con esquemas diferentes a los mencionados. La SG en estos pacientes fue significativamente más prolongada en aquellos pacientes que utilizaron adriamicina (log-rank P=5.03)(7).
Al momento de la presentación del caso en discusión, ninguna otra combinación con agentes nuevos había mostrado beneficios con respecto al CHOP.
Por lo arriba detallado, en este paciente joven con un LNH-T anaplásico a células T, sin contraindicaciones, se decidió CHOP de primera línea.
La segunda gran pregunta se refiere a si el trasplante autólogo en primera línea como tratamiento de consolidación ofrece beneficios.
Ante esta situación nos planteamos también los siguientes datos.
• Resultados de estudios prospectivos evidencian eficacia de las altas dosis de QMT y rescate con células progenitoras hematopoyéticas en 1ra. línea.
• No hay estudios randomizados que lo confirmen.
• ¿Pacientes en RC tienen mejores resultados: (“sesgo de selección”)?
• La conclusión global es que se debe mejorar el tratamiento de inducción.
• Pacientes ALK+ y IPI bajo no deben trasplantarse.
Con estos datos, en un paciente joven como el que aquí discutimos, también se podría plantear si realizar un trasplante alogénico en primera RC podría ofrecerle una SG más prolongada.
En el año 2019 el grupo alemán presentó el primer estudio de 81 pacientes en RC post CHOEP randomizados a auto vs alo trasplante en primera RC. La SG a 3 años fue superior en el grupo de trasplante autólogo(8).

Ante estos conocimientos, definimos en este paciente proceder con trasplante autólogo de células progenitoras de sangre periférica (TACPSP) en 1ra. RC luego del CHOP.
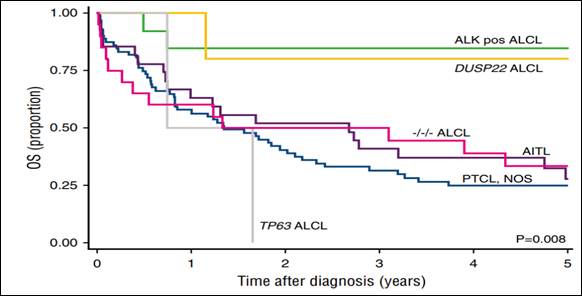
Si este paciente se presentase hoy a nuestro servicio, tendría nuevas posibilidades. Una, es la posibilidad de caracterizar a los pacientes con LNH-T anaplásico ALK - según su riesgo molecular, realizando estudios de DUSPP22 y TP63. Entendiendo que los pacientes DUSPP22 + tiene un SG a 5 años superior, cercana al 80%, y en pacientes TP63+, ésta es menor al 2% (Figura 3)(9).
Figura 3. Sobrevida global de acuerdo al perfil molecular
La otra posibilidad que tenemos hoy surge de los resultados del ECHELON 2, un trabajo prospectivo, multicéntrico, que randomiza pacientes con LNH-T CD30+ a CHOP vs brentuximab vedotin-CHP (BV-CHP), mostrando una SLP a 3 años, superior en el grupo experimental de 57 vs 44% HR: 0.71 (95% CI: 0.54-0.93; P = .0110), con una mediana de seguimiento de 36.2 meses. Esto se traduce a una diferencia en SG de 17 meses vs no alcanzada respectivamente.
La pregunta abierta que deja este protocolo es si consolidar con TACPSP post BV-CHP es seguro y eficaz.
4) Seguimiento posterior
A los 35 meses de la consolidación (septiembre 2018) el paciente se presentó a la consulta con adenopatía cervical izquierda palpable (misma localización que en el debut de enfermedad).
El PET-TC evidenciaba adenomegalia hipermetabólica cervical unilateral localizada de 14mm (SUV 4.9).
Se realizó nueva biopsia de ganglio que confirmó recaída:
Hallazgos de citometría de flujo (CMF):
En octubre de 2018 recibimos una biopsia de ganglio cervical del paciente que tenía diagnosticado un LNH-T anáplasico ALK-.
Lo primeros que hicimos por CMF fue mirar los parámetros de dispersión de luz FSC/SSC y la expresión de CD45 el antígeno pan leucocitario en analogía con lo que se hace por morfología y remedando una hematoxilina/eosina. Nos encontramos con células de gran tamaño (comparándolo con ganglios reactivos) y que expresaban intensamente CD45 en comparación con una infiltración por células de estirpe no hematológicas.
Ensayando los marcadores de estirpe linfoide, siguiendo un código de colores en los gráficos puntos azules para marcadores de células B: CD19 y CD20, puntos marrones para marcadores de célula NK relacionados con citotoxicidad: CD56, CD57 y CD11c (CD94 granzima y perforina) en ambas poblaciones fueron negativos. Pero también los marcadores para células T (en puntos verdes) CD7 CD2 CD3 CD5 CD8 todos ellos fueron negativos. Sólo expresaban CD4 de manera parcial y por lo tanto y como están descriptos en la literatura este fenotipo correspondería a células nulas. Sin embargo, la expresión de CD30 fue contundente para confirmar la infiltración de acuerdo con el antecedente y presunción diagnóstica.
Cabe destacar que la expresión de CD30 no es exclusiva de los ALCL y que, a diferencia de las células de Reed-Stemberg, por ejemplo, éstas suelen ser CD45 negativas y expresar de manera intensa CD15.
A modo de referencia vemos en el cuadro de la derecha la frecuencia de expresión reportada en la literatura para una media de 50 casos.
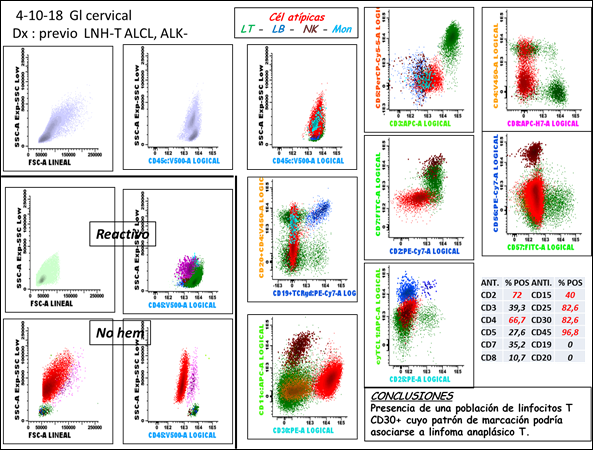
Desde el punto de vista de la CMF, salvo por la expresión de CD45, CD30, CD25, CD2 y CD4 que superan el 50%, y que en nuestro caso NO expresaba CD2 NI CD25, no podríamos asegurar que la marcación correspondiera inexorablemente a un LNH-T anaplásico, aunque podría corresponder, la interpretación diagnóstica de estos hallazgos debe hacerse en el contexto clínico/morfológico (Figura 4).
Figura 4. Hallazgos de citometría de flujo
Hallazgos de Anatomía Patológica
El estudio histopatológico, desde el punto de vista morfológico, mostró tejido ganglionar linfático difusamente infiltrado por células atípicas de gran diámetro, con moderado citoplasma eosinófilo pálido y núcleos marcadamente pleomórficos con nucléolo central prominente, destacándose frecuentes células de tipo "hallmark" con pronunciadas escotaduras nucleares (núcleos en “herradura”) (Figura 5.a). Ante este cuadro morfológico, en contexto de múltiples linfoadenopatías, el primer diagnóstico presuntivo a considerar fue una neoplasia de origen linfoide, independientemente del resultado de citometría de flujo.
Posteriormente se realizó la caracterización inmunofenotípica mediante técnica de inmunohistoquímica, realizando un primer panel de anticuerpos, con el que se llegó al diagnóstico preliminar descriptivo de linfoma de células T de alto grado histológico, observándose positividad para CD3 (marcador de diferenciación linfoide T), negatividad para CD20 (marcador de diferenciación linfoide B) (Figura 5.b) y un alto índice de proliferación (Ki67~95%). El panel complementario mostró positividad fuerte y difusa para CD30 y coexpresión para CD43, CD4 y CD2, y negatividad para CD5, CD8, CD56, Granzima B y Pax5.
El contexto clínico e histomorfológico, con presencia de frecuentes células de tipo “hallmark”, asociado a un fenotipo T (CD3+CD4+CD2+) con destacada expresión de CD30 (Figura 5.c), configuran los criterios diagnósticos del linfoma anaplásico de células grandes, haciéndose el diagnóstico diferencial con otras entidades linfoides de linaje que puede expresar CD30, como linfoma de Hodgkin clásico, linfoma de células T periférico NOS, linfoma de células T angioinmunoblástico, entre otros.
Figura 5. Hallazgos de Patología
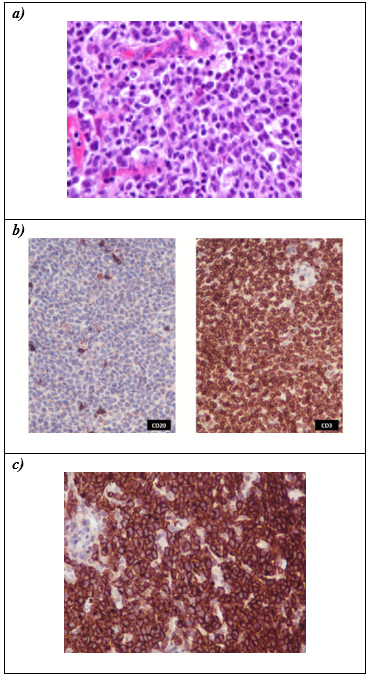
a) H&E. Proliferación difusa polimórfica con presencia de células linfoides grandes con escotaduras nucleares destacadas ("hallmark cells").
b) Positividad para CD3 (marcador de diferenciación linfoide T), negatividad para CD20 (marcador de diferenciación linfoide B).
c) CD30. Positividad fuerte y difusa (>75%).
Como paso final del algoritmo diagnóstico, se evaluó la expresión de la proteína ALK, la cual resultó negativa, llegando al diagnóstico final de linfoma anaplásico de células grandes ALK negativo (OMS 2017).
La biopsia de médula ósea al momento de la recaída descartó compromiso por enfermedad linfoproliferativa.
Se realizó búsqueda de donante. El paciente presenta HLA 3/6 con un medio-hermano (potencial donante para trasplante haploidéntico).
En ese momento se discutieron las opciones de tratamiento en ateneo institucional y se realizó el siguiente análisis del caso y conclusión:
Paciente joven con ALCL CD30 + y ALK negativo recaído post CHOP x 6 + TAMO
- Quimioterapia sola no es una opción válida.
- Opción de quimio + Talo única opción considerada curativa, aunque hay que tener en cuenta mortalidad y efectos adversos crónicos.
- Recaída localizada.
- Publicación reciente de control a largo plazo y posibilidad de cura en pacientes tratados únicamente con BV favorecieron esta opción.
- Posibilidad de rescatarlo ante nueva recaída y realizar trasplante (TALO).
5) Tratamiento de segunda línea
Se decidió realizar tratamiento con brentuximab vedotin 1,8 mg/kg. El paciente pudo completar 12 ciclos. Posteriormente el tratamiento fue suspendido por neuropatía grado 3-4 (C12: junio 2019). Se realizó evaluación posterior con PET/TC (julio 2019): Sin captación patológica. Índice de Deauville 1/5.
Discusión de la elección del tratamiento en recaída
Aproximadamente del 40% al 65% de los pacientes con linfoma anaplásico a células grandes sistémico (ALCL) desarrollan enfermedad recurrente después de terapias de primera línea. En la recaída han sido históricamente resistentes con pobres resultados a los esquemas convencionales de quimioterapia y no ha habido un estándar de cuidado establecido. Las altas dosis de quimioterapia y trasplante autólogo de células madre pueden resultar en una remisión a largo plazo en el 30% al 40% de los pacientes para aquéllos que no lo recibieron en primera línea.
Hasta hace pocos años no contábamos con opciones de tratamiento estándar para pacientes con ALCL R/R después trasplante autólogo como en el caso de nuestro paciente.
El trasplante alogénico en general es una opción para pacientes con ALCL ALK negativo que logran un RC o RP con terapias de segunda línea. Sin embargo, los riesgos y beneficios de este enfoque deben ser cuidadosamente discutidos con el paciente. La opción de trasplante alogénico se asocia con un riesgo significativo de morbilidad temprana y complicaciones tardías, pero ofrece la oportunidad de remisión a largo plazo.
Los reportes de trasplante alogénico para LNHTP recidivante o refractario se han estudiado en un grupo de pacientes con linfomas T incluyendo ALCL. Las tasas de SG a cinco años después del trasplante son de aproximadamente 50-60%, con tasas de mortalidad no relacionada al trasplante de 20-25%(10-12).
Brentuximab vedotin (BV) es un anticuerpo-fármaco conjugado dirigido a CD30 que representa hoy la mejor opción la mejor opción terapéutica entre los nuevos fármacos para el tratamiento del ALCL R/R sistémico con expresión de CD30.
La actividad de BV en ALCL fue claramente documentado por Pro et al. en un ensayo multicéntrico de fase II, donde se trataron 58 pacientes con ALCL sistémico recidivante o refractario (1,8 mg/kg cada tres semanas durante un máximo de 16 ciclos) donde se obtuvo una respuesta global 86% con una tasa de RC del 57% con una mediana de SLP de 13,3 meses(13-14).
Los efectos secundarios graves más comunes (grado 3/4) fueron neutropenia (21%), trombocitopenia (10%) y neuropatía sensorial periférica (10%).
En la actualización de 5 años de Pro et al. las respuestas globales de acuerdo al investigador fueron del 86% y las RC del 66%, (Tabla 2)(15). La duración de respuesta obtenida al BV fue independiente del estatus de ALK (Figura 6).
Tabla 2. Respuesta global y duración de la respuesta por investigador
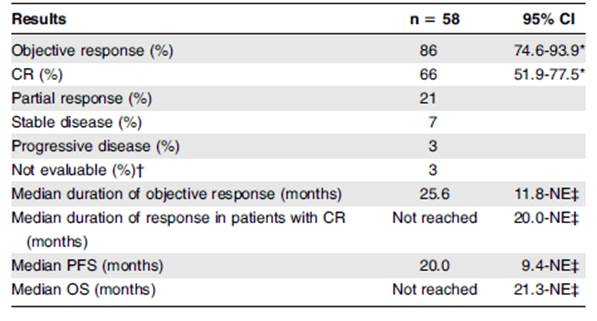 |
Figura 6. SG y SLP según el estatus de ALK
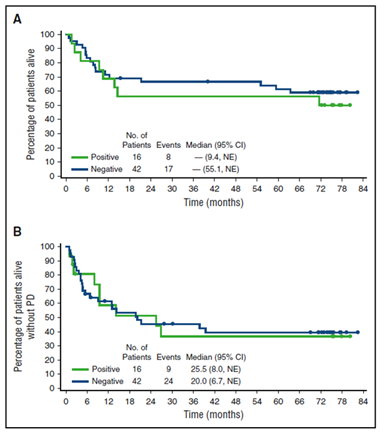 |
En los pacientes con RC (38 de 58, 66%) la SLP para los que recibieron como consolidación un trasplante fue mejor en comparación con los pacientes sin trasplante (69% vs. 48%) aunque aproximadamente la mitad de estos últimos lograron control de la enfermedad a largo plazo (Figura 6). Los pacientes que lograron RC con BV presentaron tasas de SG y SLP del 79% y 57% respectivamente con una mediana de duración de respuesta y SG no alcanzada. Aproximadamente el 91% de los pacientes que experimentaron neuropatía periférica con BV tuvieron resolución o mejoría de los síntomas.
Figura 7. SLP según estatus de TCPH
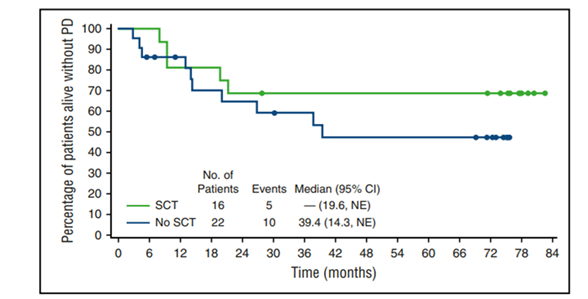
Entre los 38 pacientes que lograron RC, 16 se sometieron como consolidación a un trasplante de células hematopoyéticas. Entre estos 16 pacientes que recibieron un trasplante, los resultados a los 5 años fueron similares entre los pacientes que se sometieron a un trasplante autólogo en comparación con los pacientes que recibieron trasplante alogénico. De los 8 pacientes que recibieron un trasplante alogénico, 6 se habían sometido a un trasplante autólogo previo al ingreso al estudio. La mediana de SLP para los 22 pacientes que no procedieron al trasplante fue 39,4 meses con una tasa de SLP a 5 años del 48% (Figura 7). De los 22 pacientes que no recibieron SCT, 12 (54%) estaban vivos sin enfermedad progresiva en último seguimiento y la tasa de SG a 5 años fue del 81% con una mediana no alcanzada aún, evidenciado que es posible tener una posibilidad de control a largo plazo e incluso de estos pacientes que antaño eran de muy mal pronóstico. Incluso algunos expertos hablan de la posibilidad de cura(16).
Otros agentes -pralatrexate, romidepsin y belinostat- están aprobados por la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) para tratar el LNHTP recidivante/refractario. Ninguno tiene una actividad preferencial clara en ALCL(17-19).
En conclusión, es posible obtener remisiones completas duraderas en pacientes con LNHTP/ALCL R/R tratados con BV monoterapia y es hoy en general la segunda línea preferida para aquéllos que no hayan hecho BV de inicio generalmente de acuerdo al estudio ECHELON2 (CHP + BV). La consolidación con trasplante alogénico/autólogo deberá evaluarse de acuerdo al estado del paciente, comorbilidades y consolidación con trasplante previo.
Actualmente el paciente permanece en seguimiento. Su último control fue en febrero 2021, presentaba examen físico normal con estado funcional ECOG: 0. La neuropatía periférica secundaria a BV remitió a grado 1. Los resultados de laboratorio y tomografía computada con contraste son normales. El paciente continúa en remisión completa.
Bibliografía
1. Comparison of referring and final pathology for patients with National Comprehensive Cancer Center Network. Herrera et al. Cancer 2014
2. Vose J, Armitage J, Weisenburger D; International T-Cell Lymphoma Project. International peripheral T-cell and natural killer/T-cell lymphoma study: pathology findings and clinical outcomes. J Clin Oncol. 2008 Sep 1;26(25):4124-30.
3. Iqbal J, Wright G, Wang C, Rosenwald A, Gascoyne RD, Weisenburger DD, Greiner TC, Smith L, Guo S, Wilcox RA, Teh BT, Lim ST, Tan SY, Rimsza LM, Jaffe ES, Campo E, Martinez A, Delabie J, Braziel RM, Cook JR, Tubbs RR, Ott G, Geissinger E, Gaulard P, Piccaluga PP, Pileri SA, Au WY, Nakamura S, Seto M, Berger F, de Leval L, Connors JM, Armitage J, Vose J, Chan WC, Staudt LM; Lymphoma Leukemia Molecular Profiling Project and the International Peripheral T-cell Lymphoma Project. Gene expression signatures delineate biological and prognostic subgroups in peripheral T-cell lymphoma. Blood. 2014 May 8;123(19):2915-23.
4. Modified from: Gutierrez-Garcia: Ann Oncol. 2011; de Baaij LR, Clin Can res 2015; Federico et al BJH 2018
5. Abouyabis AN, Shenoy PJ, Sinha R, Flowers CR, Lechowicz MJ. A Systematic Review and Meta-Analysis of Front-line Anthracycline-Based Chemotherapy Regimens for Peripheral T-Cell Lymphoma. ISRN Hematol. 2011;2011:623924.
6. Schmitz N, Trümper L, Ziepert M, Nickelsen M, Ho AD, Metzner B, Peter N, Loeffler M, Rosenwald A, Pfreundschuh M. Treatment and prognosis of mature T-cell and NK-cell lymphoma: an analysis of patients with T-cell lymphoma treated in studies of the German High-Grade Non-Hodgkin Lymphoma Study Group. Blood. 2010 Nov 4;116(18):3418-25.
7. Carson KR, Horwitz SM, Pinter-Brown LC, Rosen ST, Pro B, Hsi ED, Federico M, Gisselbrecht C, Schwartz M, Bellm LA, Acosta MA, Shustov AR, Advani RH, Feldman TA, Lechowicz MJ, Smith SM, Lansigan F, Tulpule A, Craig MD, Greer JP, Kahl BS, Leach JW, Morganstein N, Casulo C, Park SI, Foss FM. A prospective cohort study of patients with peripheral T-cell lymphoma in the United States. Cancer. 2017 Apr 1;123(7):1174-1183.
8. Schmitz N, Truemper LH, Bouabdallah K, Ziepert M, Leclerc M, Cartron G, Jaccard A, Reimer P, Wagner-Drouet EM, Wilhelm M, Sanhes L, Lamy T, de Leval L, Rosenwald A, Roussel M, Kroschinsky FP, Lindemann WW, Dreger P, Viardot A, Milpied NJ, Gisselbrecht C, Wulf GG, Gyan E, Gaulard P, Bay JO, Glass B, Poeschel V, Damaj G, Sibon D, Delmer AJ, Bilger K, Banos A, Haenel M, Dreyling M, Metzner B, Keller U, Braulke F, Friedrichs B, Nickelsen M, Altmann B, Tournilhac O. A randomized phase 3 trial of auto vs. allo transplantation as part of first-line therapy in poor-risk peripheral T-NHL. Blood. 2020 Dec 17:blood.2020008825.
9. Pedersen MB, Hamilton-Dutoit SJ, Bendix K, Ketterling RP, Bedroske PP, Luoma IM, Sattler CA, Boddicker RL, Bennani NN, Nørgaard P, Møller MB, Steiniche T, d'Amore F, Feldman AL. DUSP22 and TP63 rearrangements predict outcome of ALK-negative anaplastic large cell lymphoma: a Danish cohort study. Blood. 2017 Jul 27;130(4):554-557.
13. Pro B, Advani R, Brice P et al. Brentuximab vedotin (SGN-35) in patients with relapsed or refractory systemic anaplastic large-cell lymphoma: results of a phase II study. J Clin Oncol. 2012;30(18):2190-2196.
14. Younes A, Bartlett NL, Leonard JP et al. Brentuximab vedotin (SGN-35) for relapsed CD30-positive lymphomas. N Engl J Med. 2010;363(19):1812-1821.
15. Pro B, Advani R, Brice P et al. Five-year results of brentuximab vedotin in patients with relapsed or refractory systemic anaplastic large cell lymphoma. Blood. 2017; 130(25):2709-2717.
16. Zinzani PL. ALCL: is it now a curable disease? Blood. 2017 Dec 21;130(25):2691-2692.
17. O’Connor OA, Pro B, Pinter-Brown L et al. Pralatrexate in patients with relapsed or refractoryperipheral T-cell lymphoma: results from the pivotal PROPEL study. J Clin Oncol. 2011;29(9):1182-1189.
18. Coiffier B, Pro B, Prince HM et al. Results from a pivotal, open-label, phase II study of romidepsin in relapsed or refractory peripheral T-cell lymphoma after prior systemic therapy. J Clin Oncol. 2012; 30(6):631-636.
19. O’Connor OA, Horwitz S, Masszi T et al. Belinostat in patients with relapsed or refractory peripheral T-cell lymphoma: results of the pivotal phase II BELIEF (CLN-19) study. J Clin Oncol. 2015;33(23):2492-2499.