Sistema PANDA: fórmula automatizada basada en actividad de peroxidasa
PANDA System: peroxidase and nuclear density analysis
Almirón M, Arias M
Unidad Asistencial Dr. Cesar Milstein. Ciudad de Buenos Aires
mauricionicolasalmiron@gmail.com
Palabras claves: peroxidasa,
análisis,
nuclear.
Keywords: peroxidase,
analysis,
nuclear.
Fundamento
Para realizar el recuento diferencial de leucocitos el equipo ADVIA 2120 consta de dos métodos separados: por un lado determina la actividad de la peroxidasa citoplasmática y por otro la densidad nuclear (lobularidad).
Para determinar la actividad de dicha enzima se lisan los glóbulos rojos y se utilizan reactivos específicos para distinguir entre células positivas para la peroxidasa (neutrófilos, eosinófilos y monocitos) y células negativas que incluyen linfocitos, basófilos y "células grandes no teñidas” (LUC). Para determinar la absorbancia y el tamaño se utiliza un sistema óptico basado en tungsteno. Las células absorben luz en proporción a la cantidad de peroxidasa presente, y este parámetro se relaciona con la actividad de peroxidasa representado en el eje "x" del scatter de peroxidasa. Por otro lado las células dispersan la luz en proporción a su tamaño, y este parámetro está representado en el eje "y" del gráfico (Figura 1).
Figura 1. Tamaño celular vs actividad de la peroxidasa citoplasmática.
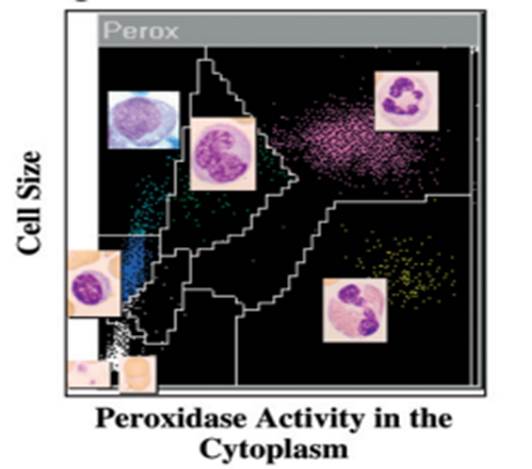
Por otro lado el canal de densidad nuclear, también llamado canal de basófilos, es el principal utilizado para informar el recuento de leucocitos. En este canal se lisan los glóbulos rojos y las plaquetas, además de eliminar la membrana plasmática de los leucocitos, excepto de los basófilos. Posteriormente se realiza un recuento de células y se clasifican de acuerdo a su tamaño, lobularidad y densidad nuclear. Este canal proporciona información valiosa respecto a la maduración nuclear debido a su lobularidad y densidad. (Figura 2).
Figura 2. Tamaño celular vs complejidad nuclear.
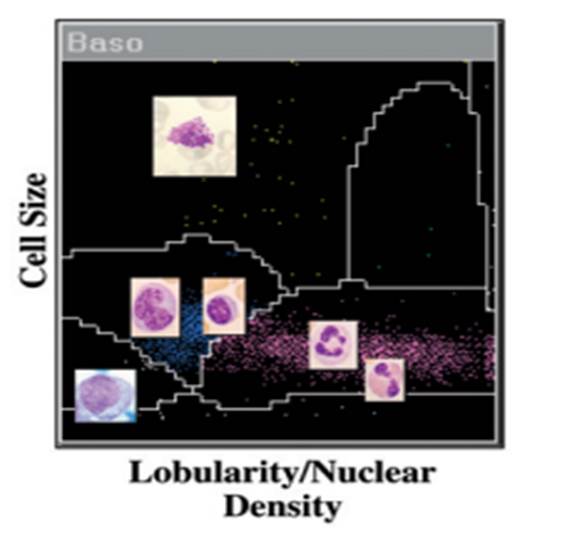
Características pre analíticas
La muestra utilizada es sangre entera anticoagulada con EDTA K3. No se requiere ayuno prolongado, aunque no se recomienda ingerir alimentos grasos en las horas previas a la extracción.
Se debe llenar el tubo hasta el enrase definido por el fabricante. Un exceso de sangre por encima de la marca presente en el tubo puede hacer que se coagule la muestra y, por ende, se generar un rechazo de la misma.
Utilidad clínica
La presencia de dos canales para determinar la fórmula diferencial provee un análisis simultáneo del contenido de mieloperoxidasa, de la densidad nuclear y del tamaño celular que se denomina método PANDA (Peroxidase And Nuclear Density Analysis), que se ha convertido en una herramienta diagnóstica junto con el inmunofenotipo y el análisis genético. Se han descripto patrones (P0 a P6) de acuerdo a un gradiente de actividad creciente de peroxidasa, donde P0 refleja una actividad nula de dicha enzima, mientras que P6 indica una actividad inusualmente aumentada de peroxidasa. De manera similar, existen 3 patrones (D0 a D2) de acuerdo a la densidad nuclear, donde D0 representa un conjunto de células mononucleares con núcleo redondo mientras en los otros dos patrones la nube celular se encuentra desplazada respecto a D0 (Figura 3).
Figura 3. Patrones formados de acuerdo a la actividad de peroxidasa (P0 a P6) y densidad nuclear (D0 a D2)
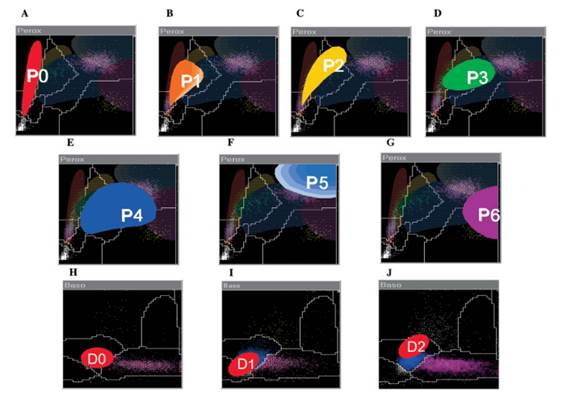
Los patrones de actividad de peroxidasa combinados con los de densidad nuclear permiten la correlación con categorías diagnósticas (Tabla 1).
De esta manera se pueden destacar algunos patrones característicos como, por ejemplo, el P6 que está asociado a una leucemia promielocítica aguda (M3) debido a la gran actividad de MPO que presentan estas células.
Otra condición que presenta un patrón característico es la deficiencia de MPO. En este caso veremos un patrón tipo P0 en caso de que el déficit sea total o un perfil P1 o P2 en aquellos pacientes en que la deficiencia sea severa o parcial respectivamente.
Tabla 1. Análisis de densidad nuclear y actividad de peroxidasa (PANDA)
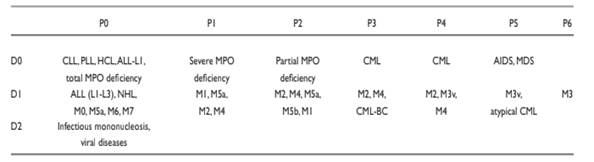
Por todo lo expuesto podemos inferir que el sistema PANDA posee ventajas particulares respecto al análisis de la fórmula leucocitaria, dado que nos brinda información valiosa en este aspecto y nos permite sospechar algunas condiciones clínicas de acuerdo al patrón obtenido en los gráficos disponibles en el equipo. Todas estas condiciones clínicas deberán ser confirmadas mediante estudios posteriores como, por ejemplo, citoquímica e inmunofenotipo.
Bibliografía
1. Harris N, Kunicka J, Kratz A. The ADVIA 2120 Hematology System: Flow Cytometry–Based Analysis of Blood and Body Fluids in the Routine Hematology Laboratory. Lab Hematol. 2005;11(1):47-61.
2. Winterbourn CC, Vissers MC, Kettle AJ. Myeloperoxidase. Curr Opin Hematol. 2000;7:53-58.
3. D’Onofrio G. PANDA: innovative classification of hematopoietic malignancies. Bloodline Rev. 2001;1:3-6.