Terapias celulares: rol de los nuevos anticuerpos
en el manejo de neoplasias linfoides
Cellular therapies: role of new antibodies in the
treatment of lymphoid neoplasias
Mahuad, C
Servicio de Hematología. Hospital Alemán, Buenos Aires
cmahuad@hospitalaleman.com
Palabras clave: linfomas
B,
inmunoterapia,
agentes
nóveles,
anticuerpos
biespecíficos,
anticuerpos
conjugados
Keywords: B
cell lymphomas,
immunotherapy,
novel
agents,
bispecific
antibodies,
antibody-drug
conjugates
Resumen
La inmunoterapia ha revolucionado el tratamiento del
cáncer. Existen diferentes enfoques, dentro de los que se incluyen los
anticuerpos monoclonales, los anticuerpos conjugados, los anticuerpos con mayor
actividad de citotoxicidad celular dependiente de anticuerpo y los llamados
anticuerpos biespecíficos, los inhibidores de puntos de chequeo y las células CART,
todos con una tasa importante de éxito. Estos nuevos anticuerpos están
estudiándose en el escenario de los linfomas no Hodgkin tanto agresivos como
indolentes, con tasas de respuesta general alentadoras que incluyen remisiones
completas. Estas respuestas se observan incluso en poblaciones de pacientes muy
pretratados, como aquéllos que han recaído luego de CART. Las toxicidades potenciales
de los BsAbs incluyen síndrome de liberación de citoquinas, la neurotoxicidad y
la reacción de llamarada tumoral, lo que requiere una serie de estrategias para
poder mitigar estos riesgos. En los siguientes párrafos se describen estos
nuevos anticuerpos, los principales resultados publicados en los últimos 5
años, su mecanismo de acción, ensayos en curso y principales eventos adversos.
Abstract
Immunotherapy has
revolutionized the treatment of cancers. There are several approaches,
including naked monoclonal antibodies, antibody-drug conjugates, monoclonal
antibodies with increased activity in antibody-dependent cytotoxicity and the
so-called bispecific antibodies, immune-checkpoint inhibitors and CART cell
therapies, all of them with an important success rate. Novel antibodies are being investigated in both
aggressive and indolent non-Hodgkin lymphoma with encouraging overall response
rates including complete remissions. These responses are seen even in heavily
pre-treated patient populations such as those who have relapsed after CART-cell
therapy. Potential toxicities include cytokine release syndrome, neurotoxicity
and tumor flare, requiring a number of strategies to mitigate these risks. The following paragraphs describe these new antibodies,
the main results published in the last 5 years, their mechanism of action,
ongoing trials and main adverse events.
Introducción
En los últimos años se han introducido nuevos anticuerpos monoclonales
(mAbs) en el tratamiento de neoplasias linfoides, predominantemente en el escenario
de la enfermedad recaída/refractaria (R/R), siendo el principal grupo de
estudio los pacientes con diagnóstico de linfoma no Hodgkin difuso a células
grandes B (LNH DCGB) que recaen o progresan al estándar terapéutico de primera
línea (1L). Para este grupo existe una clara necesidad no cubierta, y es aquí
donde comienzan a introducirse las distintas estrategias de terapias celulares.
Las células CART han sido el paradigma de estas nuevas terapias. Sin embargo,
en forma paralela, se han desarrollado múltiples mAbs que representan para
nuestro medio, quizás una estrategia con mayor posibilidad de acceso en un
futuro cercano. Dentro de los nuevos anticuerpos se incluyen los anticuerpos
conjugados a drogas (ADC), mAbs con actividad incrementada en la citotoxicidad
dependiente de anticuerpos (ADCC) y los llamados anticuerpos biespecíficos -Bispecific T-cell engagers o BiTes- (BsAbs).
Estas estrategias representan una opción terapéutica para pacientes no
elegibles para tratamientos intensivos, en quienes su enfermedad se ha
comportado como refractaria a los estándares de cuidado, sin comprometer ello
el desenlace terapéutico favorable.
En los párrafos siguientes se describen estos nuevos anticuerpos, los
principales resultados publicados en los últimos 5 años, su mecanismo de
acción, ensayos en curso y principales eventos adversos.
Anticuerpos que inducen
citotoxicidad celular dependiente de anticuerpos (ADCC)
Tafasitamab
Tafasitamab (MOR208) es un anticuerpo monoclonal anti-CD19 que utiliza una
nueva tecnología que mejora el potencial de ADCC de los anticuerpos que se
fijan al dominio FC. Los estudios preclínicos mostraron un incremento en la
actividad de las células NK cuando tafasitamab era incubado en forma conjunta
con células de pacientes con diagnóstico de LLC(1).
La eficacia clínica de tafasitamab fue evaluada en un ensayo de rama única,
multicéntrico, fase 2 (L-MIND), en el cual este anticuerpo fue administrado en
combinación con lenalidomida por hasta 12 ciclos, a pacientes con diagnóstico
de LNH DCGB R/R que no fueran candidatos a autotrasplante de médula ósea,
seguido por mantenimiento con tafasitamab. En este ensayo se observaron
respuestas a largo plazo con una tasa de respuesta global (ORR) del 60% y tasas
de remisión completa (RC) del 43%(2,3). Estos
resultados condujeron a una aprobación de emergencia por la FDA de esta
combinación en julio de 2020(4). Como evento adverso frecuente
y serio de la combinación se describió la neutropenia, con recuperación
habitual dentro de la semana de inicio de G-CSF. La trombocitopenia también fue
descripta como evento hematológico frecuente. Dentro de los eventos adversos no
hematológicos se incluyeron diarrea, eritema, fatiga, excepcionalmente grado 3
o mayores(2). Asimismo,
el estudio fase 1b FIRST-MIND mostró una tolerabilidad adecuada de la
combinación de tafasitamab/lenalidomida con R-CHOP en el escenario de 1L.
Actualmente existen abiertos, incluso en nuestro país, ensayos probando la
eficacia de esta combinación con
reclutamiento activo para el estudio MOR208C310: estudio de fase III,
multicéntrico, aleatorizado, doble ciego, controlado con placebo en el cual se
comparan la eficacia y la seguridad de tafasitamab más lenalidomida junto con R-CHOP
en comparación con R-CHOP en pacientes con diagnóstico reciente de LDCGB con
riesgo intermedio-alto y alto que no han recibido tratamiento previo.
Anticuerpos biespecíficos (BsAbs)
Los BsAbs son anticuerpos dirigidos contra un epitope blanco en la célula
tumoral y otro en la célula inmune. De este modo se facilita el acercamiento
celular, la activación de la célula efectora a través del mecanismo ADCC, de
una forma independiente del HLA(5-7). En la actualidad hay más de
100 BsAbs en desarrollo con diferentes estructuras bioquímicas y conformación. En
la mayoría de los casos, las células inmunes blanco son células T, y los
anticuerpos son dirigidos al CD3. En algunos casos, las células blanco son
células NK y macrófagos, siendo los BsAbs dirigidos al CD16A. Respecto de la
célula B tumoral, el antígeno contra el que usualmente se dirige el anticuerpo
es CD19 o CD20. Como se muestra en la figura 1, la estructura química de los
BsAbs es variable. Pueden ser clasificados en dos grupos diferentes: BsAbs sin
región Fc (conformados por dos cadenas únicas de anticuerpo unidas por un ligante)
y BsAbs con una estructura IgG-símil (tienen una región Fab y Fc en su
estructura) (Figura 1). Los
primeros tienen tamaño pequeño y vida media corta, con lo cual se necesita una
administración continua del fármaco, conformando una limitación significativa
en su uso. Los segundos, por su estructura misma, tienen un tamaño mayor y
mayor vida media, lo que permite un mayor intervalo entre las aplicaciones. La
mayoría de los BsAbs con estructura IgG-símil tienen un dominio Fc con una
actividad de fijación reducida al FcγR, lo cual disminuye la frecuencia del
síndrome de secreción de citoquinas (CRS), mejora la tolerancia, reduce las
interrupciones de los tratamientos y maximiza, de este modo, su eficacia (Tabla 1).
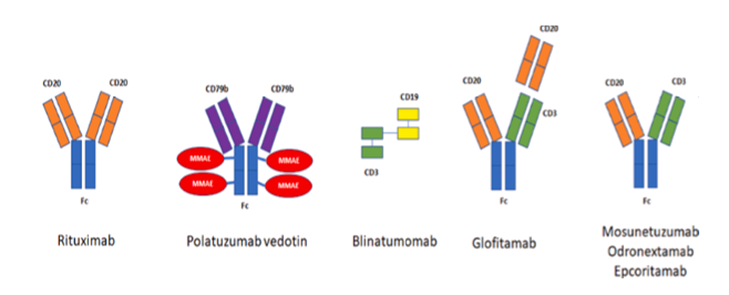
Figura 1. Estructura de los diferentes BsAbs.
MMAE= monometil-auristatina E(5)
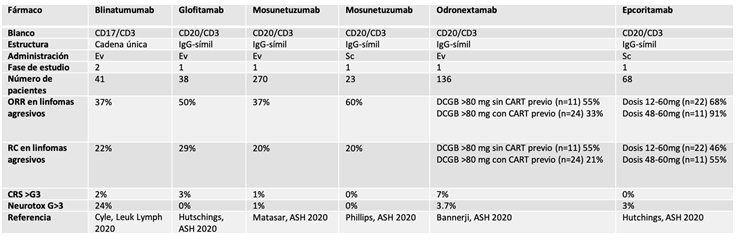
Tabla 1. Principales estudios fase 1/2 con BsAbs
en LNH DCGB(5)
Blinatumomab
Blinatumomab (MT103) fue el primer BsAb aprobado para neoplasias
hematológicas. Su aprobación inicial fue para LLA R/R y LLA B con EMR positiva(5-7). Está conformado por
una única cadena dirigida contra CD19 y CD3 (Figura 1). No contiene dominio Fc,
por lo cual su vida media es corta y requiere infusión continua. Blinatumomab
fue testeado también en LNH B, especialmente en DCGB(8). Me et al, en un
estudio fase 1, incluyeron varios subtipos de LNH B y reportaron que la mejor
dosis del anticuerpo era 60 μg/m2/día. Por debajo de estas dosis las
tasas de respuesta fueron pobres. Los eventos neurológicos fueron los
limitantes de dosis. Entre 35 pacientes tratados con esta dosis, la ORR fue 69%
(55% en los 11 pacientes con DCGB). La mediana de duración de la respuesta fue
de 404 días. Los eventos adversos neurológicos grado 3 se registraron en un 22%
de los pacientes. En otro estudio fase 2, con la mayoría de los pacientes
recibiendo una dosis progresiva del anticuerpo (9-28-112 μg/día con incremento
semanal)(9),
la tasa de respuesta en los 21 pacientes con LNH DCGB (promedio 3 líneas
previas) fue de 43% con una RC
reportada de 19% luego del primer ciclo. Nuevamente la neurotoxicidad
fue la limitante (4/5 pacientes debieron suspender el fármaco por eventos
neurológicos).
Glofitamab
Glofitamab (RG6026) es un BsAb Ig-G símil humanizado de ratón anti CD20/CD3.
Tiene una porción Fc modificada desprovista del FcγR y posibilidad de unión al
complemento, y dos sitios de unión a CD20 (derivado de obinutuzumab, modificado
por glicoingeniería) para incrementar su afinidad a los blancos CD20+ positivos (Figura 1). En un estudio
reciente fase 1, los pacientes con diagnóstico de LNH B recibieron glofitamab
en dos regímenes diferentes de dosis ascendentes (2.5-10-16 mg o 2.5-10-30 mg) para
disminuir el riesgo de CRS(10).
Glofitamab se administró en forma EV cada 3 semanas por hasta 12 ciclos. Obinutuzumab
se administró 7 días antes de la primera dosis de glofitamab (depleción de
células B), a fin de reducir la prevalencia de CRS. En el estudio se incluyeron
38 pacientes (28 con LNH agresivos: 12 con DCGB; 10 con linfomas indolentes). La
mediana de terapias previas fue 3 (rango 1-12): 71% habían sido refractarios al
último tratamiento recibido. Dentro de los 24 pacientes con linfomas agresivos
evaluables, la ORR fue 50%; RC 29%. 58 pacientes presentaron CRS, sólo uno
grado ≥ 3; ninguno presentó eventos neurológicos grado ≥ 3.
Mosunetuzumab
Mosunetuzumab (RG7828, RO7030816) también es un BsAb humanizado de ratón
heterodimérico IgG1 dirigido contra CD20/CD3 con una porción Fc modificada
desprovista del FcγR y posibilidad de unión al complemento, con un solo sitio
de unión a CD20 (Figura 1).
Mosunetuzumab se testeó como monoterapia o en combinación con esquemas tipo
CHOP u otras inmunoterapias, tanto en el escenario de enfermedad R/R como en 1L
de tratamiento. En 2019 Schuster y col. presentaron los resultados del grupo B
del estudio fase 1/1b GO29781, un ensayo de dosis escalada en el cual mosunetuzumab
fue administrado en pacientes con LNH R/R con dosis ascendentes en los días 1,
8 y 15 del C1, y luego en dosis fijas en el día 1 de los ciclos subsiguientes,
con intervalos de 21 días(11).
El 67% de los pacientes que recibieron mosunetuzumab tenían diagnóstico de
linfoma agresivo y 32%, indolente. La ORR fue 37% y la tasa de RC 20% para los
linfomas agresivos. En este estudio 30 pacientes fueron tratados con CART. Para
esta subpoblación, la ORR fue 39% y la tasa de RC 22%, mostrando eficacia en
pacientes previamente expuestos a CART. Es de destacar que a 16 meses de
iniciado el tratamiento, el 70% de los pacientes con linfomas agresivos mantenían
la respuesta. Respecto de la tolerancia, el 29% presentó CRS, pero sólo 1% CRS grado
≥ 3 y eventos adversos neurológicos grado ≥ 3.
Matasar y col.(12)
presentaron en 2020 los resultados del estudio GO29781. Mosunetuzumab se
administró en forma subcutánea cada 3 semanas por hasta 12 ciclos para reducir
la severidad de los CRS y su frecuencia, reducir la necesidad de
hospitalización y mejorar la calidad de vida del paciente. Dentro de los 22
pacientes con linfomas agresivos en quienes se evaluó eficacia, la ORR fue 69%,
y la tasa de RC 20%. Luego de una mediana de seguimiento de 7 meses, todos los
pacientes en RC excepto uno permanecían en RC. La administración SC fue bien
tolerada y no hubo CRS grado ≥ 2 con dosis < 13.5 mg. Todos los CRS
ocurrieron durante el C1 y resolvieron sin necesidad de ingreso a unidad
cerrada.
En el estudio fase 1b/2 GO40515, mosunetuzumab se administró en combinación
con CHOP (M-CHOP) por 6 ciclos totales cada 21 días, en pacientes con
diagnóstico de LNH DCGB en 1L y en algunos pacientes R/R(13). La
dosis de mosunetuzumab también fue administrada en forma progresiva para
disminuir la frecuencia de CRS. Para los pacientes con respuesta parcial o
enfermedad estable, mosunetuzumab podía administrarse hasta por un total de 11
ciclos adicionales. Dentro de los 27 pacientes con DCGB en 1L, la ORR fue 96% y
la tasa de RC 85%. No hubo CRS grado ≥ 3 ni neurotoxicidad inmunomediada
(ICANS) de ningún grado.
Mosunetuzumab está siendo evaluado en 1L en pacientes ancianos con
diagnóstico de LNH DCGB que no pueden recibir esquemas tipo R-CHOP (estudio
fase 1/2)(5).
Odronextamab
Odronextamab (REGN1979) es una BsAb heterodimérico humano basado en un IgG4
dirigido contra CD20/CD3 (monovalente para ambos antígenos). Se encuentra en
curso un estudio fase 1 que incluye pacientes con linfomas indolentes y
agresivos R/R (NCT02290951). Odronextamab se administró semanalmente hasta 12
semanas con un rango de dosis entre 0.03-320 mg. Luego, cada 2 semanas como
fase de mantenimiento(14). Se incluyeron 136 pacientes, 78 con DCGB
R/R, en su mayoría politratados. Respecto de las toxicidades, el 61%
experimentó CRS, pero sólo el 7% grado ≥ 3. El 3.7% presentó ICANS grado ≥ 3.
De los 11 pacientes con diagnóstico de DCGB que recibieron odronextamab ≥ 80 mg
sin haber recibido CART previamente, 6/11 (55%) respondieron y alcanzaron RC. De
los 24 pacientes que habían recibido previamente CART y fueron tratados con
dosis ≥ 80 mg, 8/24 (33%) respondieron y 5/24 (21%) alcanzaron RC.
Epcoritamab
Epcoritamab (GEN3013) es un BsAb heterodimérico, humanizado de ratón basado
en IgG1 dirigido contra CD20/CD3, con una modificación en la región Fc. Se
administra en forma subcutánea. En el estudio NCT03625037 en curso (fase 1/2) en
pacientes con DCGB, LF y LCM R/R, epcoritamab fue administrado en ciclos de 28
días hasta progresión de enfermedad o toxicidad inaceptable (semanalmente
durante los C1-2, cada 15 días en los C3-6 y posteriormente, mensual)(15).
Dentro de los 68 pacientes incluidos, 46 tenían diagnóstico de DCGB R/R. 59% de
los pacientes tuvieron algún grado de CRS, no hubo CRS grado ≥ 3. Dos pacientes
presentaron ICANS grado 1, 2 pacientes grado 3. En los pacientes con DCGB que
recibieron dosis entre 12 y 60 mg, la ORR fue 68%; RC 46%. En los que
recibieron dosis entre 48 y 60 mg, las mismas ascendieron a 91% y 55%,
respectivamente. Las tasas de respuesta fueron también destacables en los
pacientes con LF, LCM, así como en aquéllos que recayeron luego de CART.
Anticuerpos conjugados
Polatuzumab vedotin
Polatuzumab vedotin (DCDS4501A) es un anticuerpo anti CD79b que combina el
segmento BCR a vedotin, que es un agente disruptor del microtúbulo(6,16). En un estudio inicial fase 1,
polatuzumab mostró una ORR de 56% como monoterapia en pacientes con LNH(17). La FDA lo aprobó en
combinación con bendamustina y rituximab (BR) en 2019 luego de la publicación
del estudio GO29365, en el cual 80 pacientes con LNH DCGB R/R no aptos para
autotrasplante de médula ósea (TAMO), fueron aleatorizados 1:1 para recibir BR
o polatuzumab-BR. La tasa de respuestas completas (CR) fue superior en el grupo
tratamiento (40.0% vs 17.5%; p = 0.02), con un 15% de pacientes
mostrando respuestas duraderas de más de 20 meses(18). Los principales eventos adversos
registrados fueron fatiga, malestar gastrointestinal, anemia, neutropenia y
trombocitopenia. La combinación polatuzumab-BR se encuentra dentro de las
preferidas en las últimas guías de NCCN como segunda línea o subsecuente en el
tratamiento de LNH DCGB R/R(19).
Loncastuximab-tesirine
El loncastuximab-tesirine (ADCT-402) es un mAb dirigido contra CD19,
conjugado con tesirine, una pirrolobensodiazepina, con actividad antitumoral a
través del establecimiento de enlaces cruzados entre hebras de ADN(20,21). El uso de esta
medicación como monoterapia fue evaluada en el estudio fase 2 LOTIS-2, que
enroló 145 pacientes con LNH DCGB R/R(5,6). La mayoría de los pacientes incluidos habían
recibido al menos 3 líneas previas. Sólo una minoría había sido
autotrasplantada o había recibido CART previamente. La ORR fue 48%, habiendo
alcanzado la mitad de ellos RC. Debe destacarse que la mitad de los pacientes
que alcanzaron RC no habían progresado al momento de la presentación de los
datos del estudio(22).
Loncastuximab-tesirine fue bien tolerado. Hubo citopenias con baja incidencia en
grado 3 o mayores. Como eventos adversos no hematológicos se reportaron:
fatiga, reacciones a la infusión, náuseas y tos, mayormente grado 1-2(22).
Brentuximab vedotin (Bv)
A diferencia de los otros mAbs, Bv ganó importancia en el tratamiento de
neoplasias tanto B como T. Es un anticuerpo conjugado con vedotin, dirigido
contra CD30. El CD30 es un antígeno específico de los tejidos inmunes y se
expresa tanto en linfocitos B como T, haciéndolo un blanco terapéutico
razonable para múltiples neoplasias linfoides dentro de las que se encuentran
el linfoma de Hodgkin, ALCL, linfomas T cutáneos y DCGB(23). La eficacia de Bv en
DCGB R/R se reportó en un ensayo fase 2 que incluyó 49 pacientes con LNH DCGB
con expresión de CD30, expuestos a Bv en dosis de 1.8 mg/kg como monoterapia en
ciclos de 21 días. El tratamiento fue continuo hasta progresión de enfermedad o
toxicidad limitante. La ORR fue de 44% y CR 17%. Del mismo modo que en otras
publicaciones, no hubo correlación
entre el nivel de expresión de CD30 y las tasas de respuesta(24).
Dentro del perfil de toxicidad hematológica, la neutropenia es la más
relevante. La neuropatía periférica se encuentra dentro de los eventos adversos
específicos del Bv, que puede ser irreversible. Es usualmente sensitiva y puede
ser responsable tanto de la disminución de la dosis como de la suspensión del
fármaco, dependiendo de la severidad del síntoma (Tabla 2).
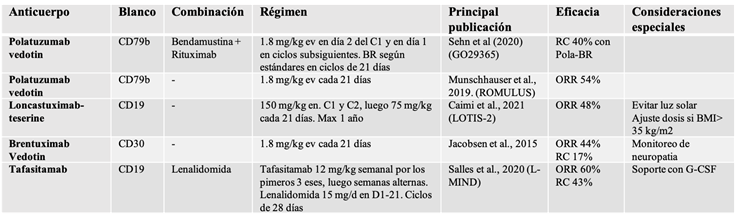
Tabla 2. Listado de nuevos anticuerpos
monoclonales en el tratamiento de neoplasias linfoides B (excluyendo BiTes). RC: remisión completa, ORR: tasa
de respuesta global
Perspectivas y conclusiones
El campo de la inmunoterapia en neoplasias linfoproliferativas se encuentra
en expansión exponencial, aumentando las opciones terapéuticas, incluso con posibilidades
de remisiones sostenidas y, en algunos casos, la curación, para pacientes que
años atrás no tenían más opción que el cuidado paliativo. El desarrollo de ADC
y BsAbs ha incrementado significativamente las opciones terapéuticas. Existen
incluso nuevas moléculas en desarrollo, nuevos blancos en células tumorales y
toxinas para ADC, así como diferentes células del sistema inmune reclutadas por
BsAbs (BsAbs dirigidos contra CD16A y reclutando células NK y macrófagos)(6,25,26).
En la tabla 3 se describen algunos de los ensayos clínicos en curso evaluando
mAbs, ADC, BsAbs, solos o en combinación con quimioterapia para LNH DCGB. La
misma expansión se observa en el escenario de los linfomas indolentes R/R.
Dentro de los principales desafíos a los que se enfrentan estas tecnologías
figuran, en primera instancia, la evaluación en etapas más tempranas del
tratamiento (1L), secuencia óptima en los algoritmos terapéuticos,
combinaciones óptimas para lograr una mayor eficacia y definir la secuenciación
correcta frente a otras terapias nóveles como las células CART. Cabe destacar
que, a la fecha, no existe comparación directa entre CART y BsAbs (Figura 2).
Por otro lado, la principal dificultad en el mundo y, sobre todo, en
nuestro medio, la representan los costos en salud y el acceso a estas nuevas
tecnologías.
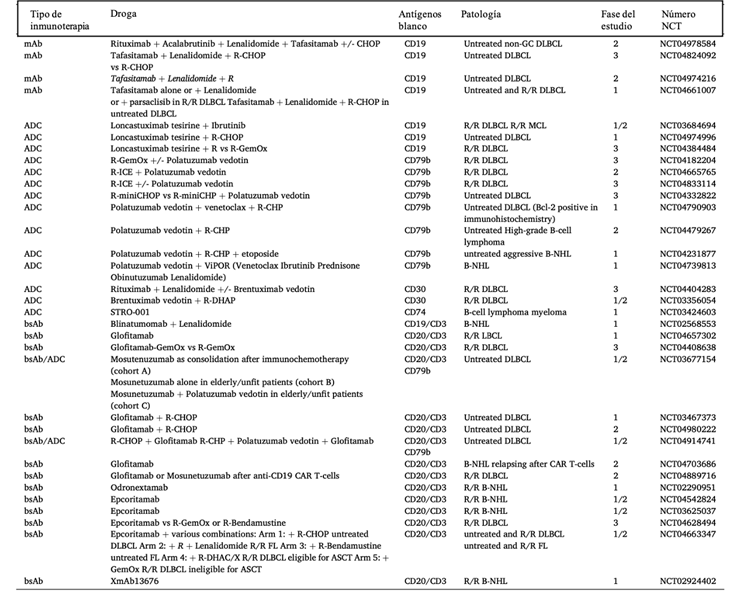 Tabla 3. Ensayos clínicos con mAbs, ADC o BiAbs en
LNH DCGB. Fuente ClinicalTrials.gov.(5)
Tabla 3. Ensayos clínicos con mAbs, ADC o BiAbs en
LNH DCGB. Fuente ClinicalTrials.gov.(5)
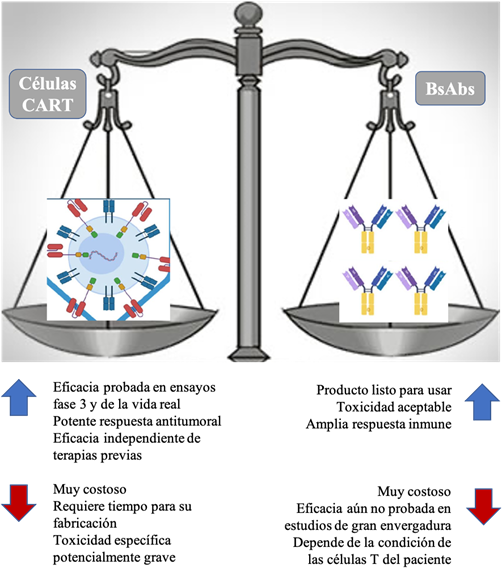
Figura 2.
Beneficios y limitaciones de las células CART y BsAbs
Bibliografía
1.
Awan FT, Lapalombella R, Trotta R, y col. CD19 targeting of chronic lymphocytic
leukemia with a novel Fc-domain-engineered monoclonal antibody. Blood 2010; 115
(6) 1204-1213.
2.
Salles G, Duell J, González Barca E, y col. Tafasitamab
plus lenalidomide in relapsed or refractory diffuse large B-cell lymphoma
(L-MIND): a multicentre, prospective, single-arm, phase 2 study. Lancet Oncol
2020; 21 (7) 978-988.
3.
Duell J, Maddocks
KJ, González-Barca E y col. Long-term outcomes from the Phase II L-MIND study of tafasitamab
(MOR208) plus lenalidomide in patients with relapsed or refractory diffuse
large B-cell lymphoma. Haematologica 2021;106
(9):2417-2426.
4.
US Food & Drug
Administration. FDA grants accelerated approval to Tafasitamab- cxix for
diffuse large B-cell lymphoma. 2020;1-2.
5.
Paillassa
J, Safa F. Novel biologic
therapies in relapsed or refractory diffuse large B cell lymphoma: CAR-T is not
the only answer. Leuk Res Rep 2021 Dec
10;17:100282.
6.
Rampotas A, Sangha G,
Colllins G. Integration of cell therapies and bispecific antibodies into the
treatment pathway of relapsed diffuse large B-cell lymphoma.Ther Adv Hematol;
2021, Vol. 12: 1-12.
7.
Castaneda-Puglianini O, Chavez JC. Bispecific antibodies for non-Hodgkin's
lymphomas and multiple myeloma. Drugs Context. 2021;10:2021-2-4.
8.
Goebeler ME, Knop S, Viardot A y col. Bispecific T-Cell
Engager (BiTE) Antibody Construct Blinatumomab for the Treatment of Patients
With Relapsed/Refractory Non-Hodgkin Lymphoma: Final Results From a Phase I
Study. J Clin Oncol 2016; 34 (10) 1104-1111.
9.
Viardot
A, Goebeler ME, Hess G y col. Phase 2 study
of the bispecific T-cell engager (BiTE) antibody blinatumomab in
relapsed/refractory diffuse large B-cell lymphoma. Blood 2016; 127 (11) 1410-1416.
10. Hutchings M, Carlo-Stella C, Bachy E y col.
Glofitamab step-up dosing induces high response rates in patients with
hard-totreat refractory or relapsed non-Hodgkin lymphoma, Blood 136 (2020) 46-48.
Nov (Supplement 1).
11. Schuster SJ, Bartlett NL, Assouline S y col.
Mosunetuzumab induces complete remissions in poor prognosis non-Hodgkin
lymphoma patients, including those who are resistant to or relapsing after
chimeric antigen receptor T-cell (CAR-T) therapies, and is active in treatment
through multiple lines. Blood 2019; 134 (Supplement 1).
12. Matasar M,Chan Yoon Chea, Dok Hyun Yoon y col.
Subcutaneous Mosunetuzumab in relapsed or refractory B-cell lymphoma: promising
safety and encouraging efficacy in dose escalation cohorts. Blood 2020; 136
(Supplement 1) 45-46.
13. Phillips TJ, Olszewski AJ, Munoz J y col.
Mosunetuzumab, a novel CD20/CD3 bispecific antibody, in combination with CHOP
confers high response rates in patients with diffuse large B-cell lymphoma.
Blood 2020;136 (Supplement 1) 37-38.
14. Bannerji
R, Allan JN, Arnason JE y col. Odronextamab
(REGN1979), a human CD20 x CD3 bispecific antibody, induces durable, complete
responses in patients with highly refractory B-cell non-Hodgkin lymphoma,
including patients refractory to CAR T therapy. Blood 2020;136 (Supplement 1)
42-43.
15. Hutchings M, Mous R, Clausen MR, P y col.
Subcutaneous Epcoritamab induces complete responses with an encouraging safety
profile across relapsed/refractory B-cell non-Hodgkin lymphoma subtypes,
including patients with prior CAR-T therapy: updated dose escalation data.
Blood 2020;136 (Supplement 1) 45-46.
16. Pfeifer M, Zheng
B, Erdmann T y col. Anti-CD22
and anti-CD79B antibody drug conjugates are active in different molecular
diffuse large B-cell lymphoma subtypes. Leukemia 2015; 29 (7) 1578-1586.
17. Palanca-Wessels MCA, Czuczman M, Salles G y col. Safety and activity of the anti-CD79B
antibody-drug conjugate polatuzumab vedotin in relapsed or refractory B-cell
non-Hodgkin lymphoma and chronic lymphocytic leukaemia: a phase 1 study. Lancet
Oncol 2015; 16 (6) 704-715.
18. Sehn L, Herrera
AF, Flowers CR y col. Polatuzumab Vedotin in Relapsed or Refractory
Diffuse Large B-Cell Lymphoma. J Clin Oncol 2020; 38 (2) 155-165.
19. National Comprehensive Cancer Network. B-Cell
Lymphomas (Version 1.2022-2.2022).
20. Zammarchi F, Corbett
S, Adams L y col. ADCT-402, a PBD dimer-containing antibody drug
conjugate targeting CD19-expressing malignancies. Blood 2018; 131 (10) 1094-1105.
21. Hartley JA, Flynn MJ, Bingham JP y col. Pre-clinical pharmacology and mechanism of action of SG3199, the
pyrrolobenzodiazepine (PBD) dimer warhead component of antibody-drug conjugate
(ADC) payload tesirine. Sci. Rep 2018; 8 (1) 1-10.
22. Caimi PF, Ai W, Alderuccio JP y col. Loncastuximab
tesirine in relapsed or refractory diffuse large B-cell lymphoma (LOTIS-2): a
multicentre, open-label, single-arm, phase 2 trial. Lancet Oncol 2021; 22 (6) 790-800.
23. Chiarle R, Prolla A, Prolla G, Gong J, Thorbecke
G, Inghirami G col. CD30 in normal and neoplastic cells. Clin. Immunol 1999;
Vol. 90 157-164.
24. Jacobsen ED, Sharman JP, Oki Y y col. Brentuximab vedotin demonstrates objective responses in a phase 2 study
of relapsed/refractory DLBCL with variable CD30 expression. Blood 2015; 125 (9) 1394-1402.
25. Einsele H Borghaei
H, Orlowski RZ y col. The BiTE (bispecific T-cell engager) platform:
Development and future potential of a targeted immuno-oncology therapy across
tumor types. Cancer; 2020 Jul
15;126(14):3192-3201.
26. Salvaris R Ong J,
Gregory GP. Bispecific Antibodies: A Review of Development, Clinical
Efficacy and Toxicity in B-Cell Lymphomas. J. Pers. Med. 2021, 11 (5): 355.