Requerimientos
analíticos y preanalíticos para el análisis de ferritina
Analytical and preanalytical requirements for ferritin analysis
A. Bertoncin; M.
Dicugno
Laboratorio Central del Hospital
Británico de Buenos Aires
abertoncin@hbritanico.com.ar
Palabras claves: ferritina,
hierro,
métodos.
Keywords: ferritin,
iron,
methods.
Introducción
La disponibilidad de métodos
sensibles para medir la ferritina sérica ha aumentado la posibilidad de
detectar la insuficiencia y sobrecarga de hierro. Desde el punto de vista
clínico, las concentraciones bajas de ferritina pueden ayudar en el diagnóstico
de la anemia ferropénica, mientras que las concentraciones elevadas se
encuentran en casos de enfermedades infecciosas o inflamatorias, por ser una
proteína reactante de fase aguda. Esta proteína también está elevada en casos
de sobrecarga de hierro, ya sea anemia hemolítica, sideroblásticas, múltiples
transfusiones, hemocromatosis y en pacientes con hepatopatías.
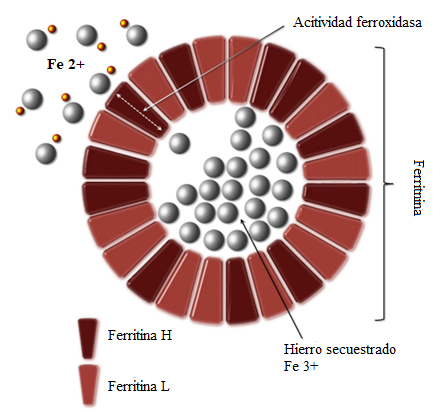
Figura 1. Estructura de la
ferritina
El hierro en estado ferroso es
tóxico en los sistemas celulares debido a su capacidad para generar especies
reactivas (mostradas como esferas amarillas) que pueden dañar directamente el
ADN y las proteínas(1).
Fundamento del
ensayo
La
ferritina puede medirse a través de diversos tipos de inmunoensayos en los que
varía la tecnología que se utiliza para la detección del inmunocomplejo
antígeno-anticuerpo. Entre éstos se encuentran principalmente los ensayos
radiométricos (RIA/IRMA -en desuso-), los no radiométricos
(inmunofluorescencia, quimioluminiscencia, electroquimioluminiscencia) y los
ensayos por aglutinación (inmunoturbidimetría o nefelometría).
Los
ensayos inmunométricos (sándwich) requieren, en primer término, que los anticuerpos
anti-ferritina inmovilizados en una fase sólida (tubo, perlas, fibra de vidrio
o partículas paramagnéticas) reaccionen con la ferritina y, luego, sean
lavados. Posteriormente se agrega un exceso de un segundo anticuerpo anti-ferritina
marcado con un trazador luminiscente o fluorescente, que se unirá en forma
directamente proporcional con las moléculas de ferritina capturadas en la
primera etapa de la reacción. En el caso de los ensayos inmunoturbidimétricos,
la ferritina presente en la muestra reacciona con partículas de látex
sensibilizadas con anticuerpos anti-ferritina humana, produciendo aglutinación.
La turbidez causada es proporcional a la concentración de ferritina en la
muestra y puede ser medida por turbidimetría o nefelometría.
La tabla
1 muestras las distintas especificaciones técnicas, las características
preanalíticas y los valores de referencia propuestos de los ensayos más
utilizados. Se comparan los valores de precisión a través de CV% total a
niveles de decisión médica provisto por los insertos de las distintas marcas
comerciales.
Si bien no existe un método de
laboratorio patrón oro para la determinación de ferritina, la recomendación
internacional sugiere elegir un método que cuente con calibradores comerciales
trazables a un material de referencia internacional (p. ej. patrón de la OMS). Se puede observar en la tabla 1 que los
métodos por ECLIA y quimioluminiscencia muestras un rango lineal mayor y un límite de detección menor que los métodos por
turbidimetría.
Se destaca la importancia en el
procesamiento de controles internos al menos una vez cada 24 horas, cada día de
su uso, como también la participación de encuestas de control externo de
calidad.
Tabla 1.
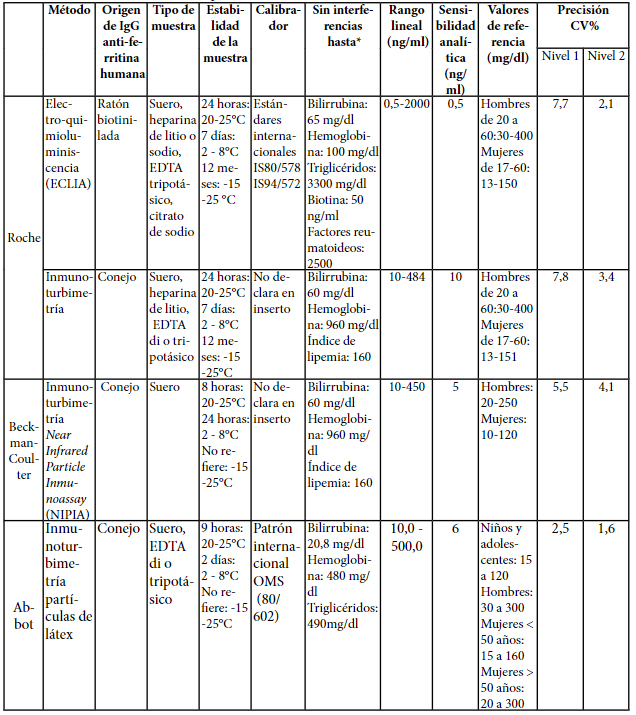
*: Referirse a la
bibliografía de Young para los efectos de las drogas en el presente método
Valores de referencia
Las concentraciones de ferritina
son altas al nacer y continúan aumentando hasta la edad adulta. Sin embargo, a
partir de la adolescencia, los varones tienen valores más altos que las mujeres
y esta tendencia persiste hasta la edad adulta tardía. Los valores entre los
hombres alcanzan su punto máximo entre los 30 y los 39 años y, luego, tienden a
permanecer constantes hasta los 70 años. Entre las mujeres, en cambio, los
valores de ferritina sérica permanecen relativamente bajos hasta la menopausia
y luego aumentan.
Además de las variaciones según la
edad y el sexo, los valores son afectados por factores geográficos,
alimenticios y medioambientales. Por estos motivos es recomendable que cada
laboratorio establezca sus propios valores de referencia o valide con su propia
población los provistos por el proveedor (Tabla 1). Y en el seguimiento de
pacientes se recomienda que, una vez seleccionado un método, se utilice el
mismo durante las diferentes medidas de seguimiento.
Utilidad clínica
Concentraciones
disminuidas de ferritina
Las concentraciones de ferritina
inferiores a 12 ng/ml son un indicio altamente específico de la ausencia de
reservas de hierro según la Organización Mundial de Salud. Aunque la biopsia de
médula ósea con tinción de hierro sigue siendo el patrón oro para el
diagnóstico de deficiencia de hierro, es un método subjetivo, semicuantitativo,
invasivo y no habitual para realizar frente a una sospecha de anemia
ferropénica. Por fuera de este diagnóstico sólo se conocen dos condiciones que
reducen la ferritina sérica: el hipotiroidismo y la deficiencia de ascorbato.
En pacientes con anemia ferropénica
y con inflamación o infección subyacente los valores de ferritina pueden verse
falsamente aumentados por ser una proteína reactante de fase aguda y no por
tener un aumento de depósitos. Se sugiere utilizar valores de corte superior a aproximadamente 40 ng/ml para
excluir la deficiencia de hierro en la mayoría de los pacientes, mientras que
un nivel superior a 70 ng/ml para excluir la deficiencia de hierro en pacientes
con inflamación.
Concentraciones
aumentadas de ferritina
El aumento de la síntesis de
ferritina puede indicar aumento en las reservas de hierro del organismo o ser
una consecuencia de su característica de reactante de fase aguda.
Dentro del primer grupo, la
sobrecarga de hierro ocurre por una absorción anormal o una administración
excesiva: terapias con hierro oral o transfusiones múltiples. Las mediciones de
la ferritina sérica son útiles en el seguimiento del control del incremento de
los depósitos férricos en estos pacientes bajo terapia y para determinar cuándo
se puede interrumpir la misma, sin llegar a un nivel de sobrecarga o, en el
caso de las terapias con trasfusiones crónicas (ej.: talasemia mayor),
complementar la terapéutica con un quelante de hierro.
En cuanto al metabolismo del
hierro, el único punto de regulación es la absorción, ya que no existe un
mecanismo de excreción del mismo. La hemocromatosis es un trastorno autosómico
recesivo que expresa la proteína HFE alterada que provoca una mayor absorción
de hierro depositándose en hígado y corazón. Esto lleva a una insuficiencia
cardíaca y hepática progresiva. El dosaje de ferritina es una estrategia recomendada
frente a la sospecha de la enfermedad y como seguimiento de la flebotomía
terapéutica.
Otra de las enfermedades
caracterizadas por aumento de depósitos de ferritina son las anemias
sideroblásticas, pero al ser su causal una eritropoyesis ineficaz, a diferencia
de la hemocromatosis genética, el depósito de hierro se produce en los
macrófagos de la médula ósea.
Por último, la ferritina sérica es
reconocida como un reactante de fase aguda y se encuentra elevada de manera
inespecífica en una amplia gama de afecciones inflamatorias, incluidas la
enfermedad renal crónica, la artritis reumatoidea y otros trastornos
autoinmunes, infecciones agudas y malignidad. La ferritina elevada en estos estados refleja un aumento del
almacenamiento total de hierro en el cuerpo, pero, paradójicamente, estos
depósitos están secuestrados y no están disponibles para la hematopoyesis. Se
presume que esta deficiencia relativa de hierro (en la inflamación y la
malignidad) se desarrolló como un mecanismo de defensa para restringir la
utilización del hierro sérico por parte de patógenos y tumores.
Uno de estos casos es la anemia de
los procesos crónicos (APC), donde se tienen valores de ferremia y saturación
de transferrina disminuida; sin embargo, para realizar el diagnóstico
diferencial con la anemia ferropénica se utiliza la ferritina ya que en la APC
se encuentra elevada.
En el caso de los pacientes con enfermedad renal crónica, la
ferritina sérica no es un buen marcador de hierro biodisponible, porque suelen
presentar valores elevados debido a la inflamación crónica de estos pacientes. La
deficiencia absoluta de hierro se define utilizando otra medida de laboratorio
como saturación de transferrina <20% o el receptor soluble a la
transferrina.
Por último, las inflamaciones
sistémicas consecuentes a enfermedades autoinmunes como lupus o por infecciones
virales, particularmente el virus de Epstein -Bar, también cursan con valores
constantemente elevados de ferritina y pueden desencadenar en un síndrome hemofagocítico,
siendo una de sus características diagnósticas la hiperferritinemia (valores
mayores de 500 ng/dl).
Bibliografía
1. Knovich
MA, Storey JA, Coffman LG, Torti SV, Torti FM. Ferritin for the clinician.
Blood Rev. 2009 May;23(3):95-104.
2. Garcia-Casal
MN, Peña-Rosas JP, Urrechaga E, Escanero JF, Huo J, Martinez RX, Lopez-Perez L.
Performance and comparability of laboratory methods for measuring ferritin
concentrations in human serum or plasma: A systematic review and meta-analysis.
PLoS One. 2018 May 3;13(5):e0196576.
3. World
Health Organization. Serum ferritin concentrations for the assessment of iron
status and iron deficiency in populations. Geneva: World Health Organization,
2011.
4. Wang W, Knovich MA, Coffman LG, Torti FM, Torti SV. Serum
ferritin: Past, present and future. Biochim Biophys Acta. 2010
Aug;1800(8):760-9.
5. Young
DS. "Effects of Drugs on Clinical Laboratory Tests", AACC Press, 5th
ed., 2000.

