Tiempo de lisis del coágulo en plasma libre de plaquetas
Clot lysis time in platelet-free plasma
Rodríguez D1-2; Hidalgo P1
1. Laboratorio de trombosis y hemostasia, Servicio de Laboratorios Clínicos, Red de Salud UC-CHRISTUS, Santiago, Chile.
2. Departamento de Laboratorios Clínicos, Facultad de Medicina, Pontificia Universidad Católica de Chile.
Fundamento
Este ensayo modificado, permite una evaluación detallada de la capacidad de formación y degradación de la fibrina(1). Plasma libre de plaquetas (PLP) se mezcla con un activador de la coagulación, fosfolípidos y calcio para inducir la formación de fibrina. Simultáneamente se añade t-PA u otro activador del plasminógeno para inducir la lisis del coágulo. El ensayo utiliza el principio de turbidimetría para la detección, aumentando la turbidez de la muestra con la formación de fibrina y disminuyendo con su lisis. La absorbancia se registra a intervalos de tiempo continuos por un período determinado, resultando en la formación de una curva que permite la evaluación de la actividad fibrinolítica plasmática
Características preanalíticas
Se sugiere elegir vena en la zona antecubital para la toma de muestra. Con aplicación de torniquete 3 a 5 centímetros sobre el sitio a puncionar no más de 30 segundos. Obtener muestra de sangre venosa en tubo con citrato de sodio 0.109 M 3.2% respetando relación sangre anticoagulante (1:9) señalada en el tubo. Invertir el tubo para la completa homogenización. Iniciar el procesamiento dentro de 4 horas de la flebotomía. Centrifugar a 3500 RPM por 10 minutos a temperatura ambiente. Luego de separar, se realiza una segunda centrifugación a 11000 RPM por 5 minutos a temperatura ambiente para obtener el plasma libre de plaquetas (PLP). La muestra debe ser alicuotada a tubos secundarios y congelada a -80 °C inmediatamente luego de procesar, manteniéndola a esta temperatura hasta su análisis. Se espera una estabilidad de como mínimo 1 año en estas condiciones.
Consideraciones analíticas
Reactivos
· Tromboplastina (TF) recombinante humana, (RecombiPlasTin 2G, IL)
· t-PA recombinante humano 1 mg/mL (Actilyse, Boehringer Ingelheim)
· Fosfolípidos 500 µM (Rössix, Mölndal, Sweden)
· Buffer HEPES
· Buffer HEPES calcio
· Buffer HEPES BSA
· Control pool de plasma normal
Materiales especiales y equipos
· Placas de microtitulación de poliestireno con fondo plano
· Re-pipeteador o pipeta multicanal
Preparación de soluciones
Buffer HEPES
|
Componente |
Peso molecular (g/mol) |
Concentración |
CAS |
|
HEPES C8H18N2O4S1 |
238.3 |
0.02 M |
7365-45-9 |
|
NaCl |
58.44 |
0.15 M |
7647-14-5 |
|
Disolver en agua destilada. Ajustar pH a 7.4 con NaOH 6N. Refrigerar y almacenar a 4°C máximo 3 meses. |
|||
Buffer HEPES calcio
|
Componente |
Peso molecular (g/mol) |
Concentración |
CAS |
|
HEPES C8H18N2O4S1 |
238.3 |
0.02 M |
7365-45-9 |
|
NaCl |
58.44 |
0.15 M |
7647-14-5 |
|
CaCl2 di hidratado |
147.02 |
0.2 M |
10043-52- 4 |
|
Disolver en agua destilada. Ajustar pH a 7.4 con NaOH 6N. Refrigerar y almacenar a 4°C máximo 3 meses. |
|||
Buffer HEPES BSA
|
Componente |
Peso molecular (g/mol) |
Concentración |
CAS |
|
HEPES C8H18N2O4S1 |
238.3 |
0.02 M |
7365-45-9 |
|
NaCl |
58.44 |
0.15 M |
7647-14-5 |
|
Albúmina sérica bovina liofilizada (>98% pureza) |
- |
1% |
- |
|
Disolver en agua destilada. Ajustar pH a 7.4 con NaOH 6N. Refrigerar y almacenar a 4°C máximo 1 mes. |
|||
Preparación de reactivos. Realizar las siguientes soluciones justo antes de realizar el ensayo (menos de 20 minutos) según el esquema.
|
Solución de t-PA en HEPES-BSA [870 ng/mL] |
Diluir 40 µL de r-TPA en 1960 µL de buffer HEPES BSA Posteriormente 150 µL de la solución anterior en 3300 µL. |
|
TF en HEPES [1:49875*] |
Diluir 10 µL de TF en 1320 µL de buffer HEPES. Posteriormente 10 µL de la solución anterior en 2450 µL. |
|
Fosfolípidos en HEPES [60 µM] |
Diluir 48 µL de fosfolípidos en 352 µL de buffer HEPES. |
|
*Concentración final de reacción |
|
Realizar la solución de mezcla de reacción con TF en HEPES, fosfolípidos en HEPES y buffer HEPES en una relación 2:1:1.
Organizar la placa del ensayo. Se debe incluir el control y cada muestra de paciente en octuplicado. Descongelar muestras y control en baño termorregulado a 37°C por 5 minutos. Añadir en cada pocillo (Figura 1):
a) 70 µL de PLP de muestra o control
b) 40 µL de mezcla de reacción
c) 20 µL de r-TPA
d) 20 µL de buffer HEPES calcio
Insertar la placa en el lector y dar inicio al protocolo de lecturas (cinética lenta, absorbancia 405 nm por 0.1 segundos. Agitación lenta. Medir cada placa 100 veces cada minuto, por 100 minutos. Demora entre lecturas de 0 s y temperatura 37°C).
Obtener los datos en una planilla en una hoja de cálculo, graficar las curvas (tiempo contra absorbancia) y calcular los siguientes datos de cada pocillo como el gráfico de ejemplo (Figura 2).
Realizar cálculo de promedio, desviación estándar y coeficiente de variación expresado en porcentaje (CV). Revisar cada curva y excluir las que tienen un comportamiento aberrante. Se recomienda validar ensayos con CV menores a 10% entre los replicados de cada muestra o control, así como construcción de rangos de referencia locales.
Utilidad clínica
La fibrinólisis es un proceso continuo de degradación del coágulo de fibrina, estrictamente regulado para mantener el equilibrio entre la formación y la degradación de la fibrina(2). El tiempo de lisis es inversamente proporcional a la actividad fibrinolítica plasmática. El deterioro de la capacidad fibrinolítica también puede contribuir al estado hipercoagulable (hipofibrinólisis) con riesgo de trombosis(3) o a tendencia hemorrágica(4) (hiperfibrinólisis). Esta versión modificada del tiempo de lisis del coágulo(1) permite evaluar en forma detallada la capacidad de formación de fibrina y fibrinólisis, cuyos resultados orientan a diversos significados resumidos en la siguiente tabla de hallazgos.
Bibliografía
1. Larsen JB, Hvas AM. Fibrin Clot Formation and Lysis in Plasma. Methods Protoc. 2020;3(4):67.
2. Longstaff C, Kolev K. Basic mechanisms and regulation of fibrinolysis. J Thromb Haemost. 2015;13 Suppl 1:S98-S105.
3. Lisman T. Decreased Plasma Fibrinolytic Potential As a Risk for Venous and Arterial Thrombosis. Semin Thromb Hemost. 2017;43(2):178-184.
4. Saes JL, Schols SEM, van Heerde WL, Nijziel MR. Hemorrhagic disorders of fibrinolysis: a clinical review. J Thromb Haemost. 2018 May 30.
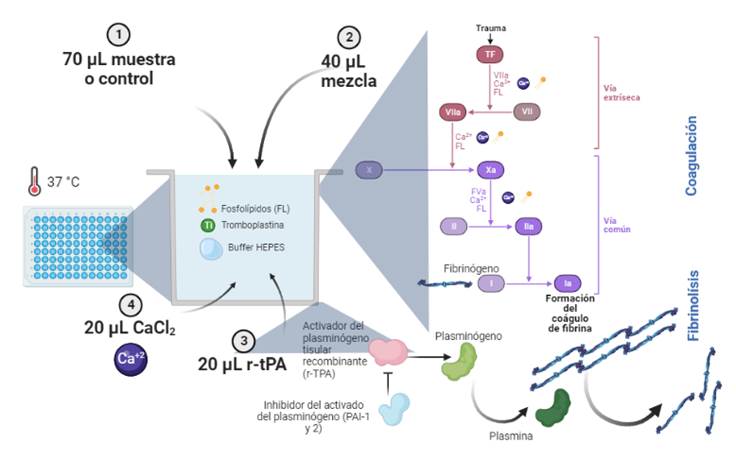
Figura 1.
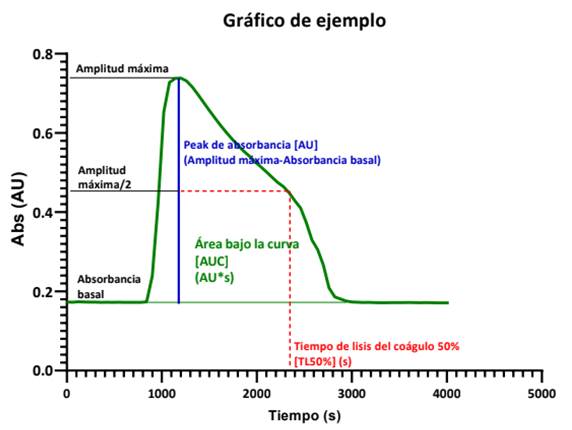
Figura 2.
|
Tabla de hallazgos |
||
|
Parámetro |
Representa |
Interpretación |
|
Absorbancia Máxima (AU) 0.241-0.843 |
Concentración máxima de fibrina alcanzada |
↑: aumento en la actividad procoagulante. - Elevación del fibrinógeno plasmático |
|
↓: disminución de la actividad procoagulante - Posible disminución de concentración plasmática de factores de la coagulación o fibrinógeno |
||
|
Integral (AU x s) 935-2774 |
Formación neta de fibrina. Balance entre formación y lisis de fibrina |
↑: aumento en la actividad procoagulante. - Disminución de la actividad de anticoagulantes endógenos - Disminución de la capacidad fibrinolítica |
|
↓: disminución de la actividad procoagulante o de la estabilidad del coágulo. - Posible disminución de concentración plasmática de factores de la coagulación, factor XIII o fibrinógeno - Aumento de la capacidad fibrinolítica |
||
|
Tiempo de lisis 50% (s) 433-1181 |
Tiempo desde que se alcanza la concentración máxima de fibrina hasta la lisis del 50% del coágulo |
↑: disminución de la actividad fibrinolítica: - Disminución del plasminógeno circulante - Elevación de PAI-1 y/o TAFI - Tratamiento antifibrinolítico - Disminución del factor XIII |
|
↓: elevada actividad fibrinolítica: - Concentraciones plasmáticas de t-PA o u-PA elevadas |
||
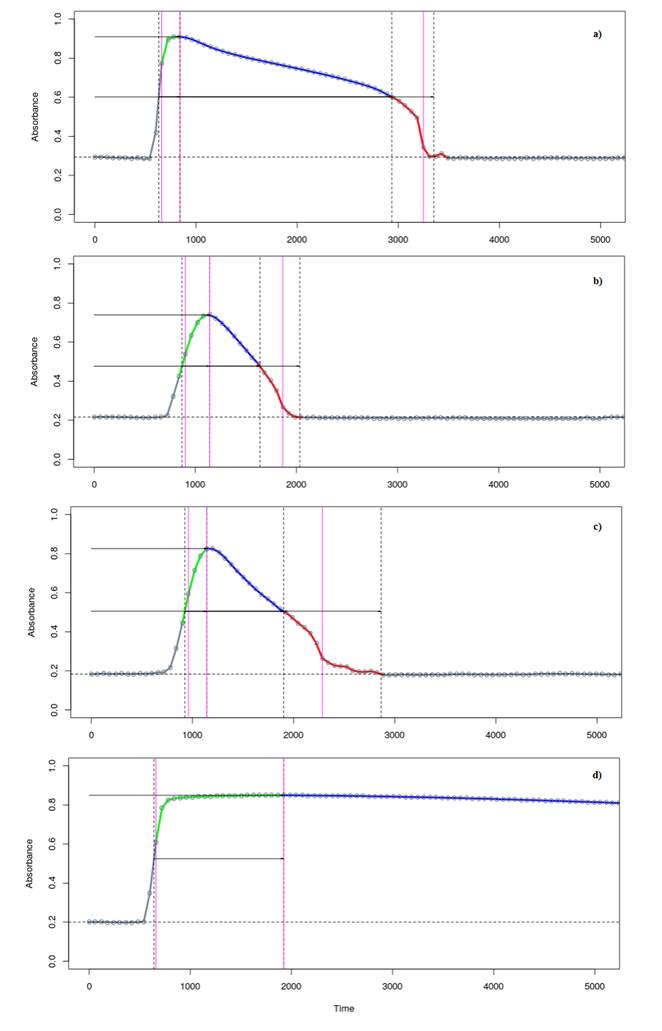
Figura 3, a) Hiperfibrinólisis b) Hiperfibrinólisis c) Normal d) Efecto de ácido tranexámico