Validación de un método para la cuantificación plasmática de emicizumab
Validation of a method for plasma quantification of emicizumab
Sueldo E, Annetta E, Frontroth J, Cervio C, Bianco B, Sciuccati G, Hepner M.
Laboratorio de Hemostasia y Trombosis, Servicio de Hematología y Oncología del Hospital de Pediatría “Prof. Dr. Juan P. Garrahan”
Ciudad Autónoma de Buenos Aires, Argentina
https://orcid.org/0000-0002-5466-2953 E SUELDO
https://orcid.org/0009-0009-0112-4279 Eliana Annetta
https://orcid.org/0000-0001-6901-584X Juan Pablo Frontroth
https://orcid.org/0009-0009-0678-8437 Carolina cervio
https://orcid.org/0009-0004-9978-8527 Belén Bianco
https://orcid.org/0009-0004-9546-5018 Gabriela Sciuccati
https://orcid.org/0009-0005-6345-6667 Mirta Hepner
Palabras claves:Validación
FVIII coagulométrico en una etapa modificado
Emicizumab
Hemofilia A
Keywords: Validation
Modified One Stage FVIII Assay
Emicizumab
Hemophilia A
Resumen
Introducción: El emicizumab (Hemlibra®, ROCHE) es un anticuerpo monoclonal IgG4 bi-específico, recombinante y humanizado, que mimetiza la función del FVIIIa. Su administración por vía subcutánea es eficaz y segura en la prevención de hemorragias en pacientes con hemofilia A severa con o sin inhibidor. Si bien el emicizumab ha sido aprobado con un régimen de administración basado en el peso corporal y sin un monitoreo de los niveles plasmáticos, la cuantificación plasmática de emicizumab puede ser útil en distintas circunstancias clínicas y de investigación. Debido a que en Argentina aún no están disponibles los calibradores y controles comerciales específicos de emicizumab, hemos validado un método para la cuantificación plasmática de emicizumab (Epc), basado en la medición de FVIII por método coagulométrico en una etapa modificado (modFVIIIcoag), utilizando calibradores y controles preparados “in-house”. Materiales y métodos: para la Epc se utilizó una predilución de la muestra 1/80 con buffer Owren Koller. El calibrador “in-house” de emicizumab (150 μg/mL de emicizumab) se preparó agregando emicizumab de 150 mg/ml a un plasma deficiente en FVIII. Se prepararon dos niveles de control “in-house” y una curva de calibración de 6 puntos. Los procedimientos de validación se realizaron en un STA Compact Max2 (Diagnostica Stago): Repetibilidad; se procesaron los controles 20 veces en la misma corrida analítica, Imprecisión Intra-Laboratorio; se procesaron los controles por triplicado durante 5 días, Linealidad; 11 niveles medidos por triplicado, Límite de cuantificación; 15 mediciones de un plasma deficiente de FVIII comercial, Bias; a partir de un programa de evaluación externa de calidad (UK NEQAS). Se evaluó la interferencia del FVIII y rFVIIa en Epc, y de emicizumab en otras determinaciones de hemostasia. Resultados: Epc mostró una imprecisión y un sesgo aceptables, un rango lineal de 5-150 µg/ml y un límite de cuantificación de 5 µg/ml de emicizumab. En los estudios de interferencia se encontró que el FVIII interfiere con Epc pero no así el rFVIIa. Emicizumab acortó los valores del TTPa por debajo del límite inferior del intervalo de referencia local, mientras que el FVIII medido por método cromogénico con componentes de origen bovino no fue afectado. El método coagulométrico de una etapa de FVIII fue falsamente aumentado y mostró una fuerte correlación lineal con Epc en este sistema reactivo/instrumento. Discusión: El ensayo modFVIIIcoag automatizado “in-house” permite la cuantificación plasmática de emicizumab mediante un método sencillo, reproducible, de bajo costo y de fácil integración en los procesos de rutina.
SummaryIntroduction: Emicizumab (Hemlibra®, ROCHE) is a bispecific, recombinant and humanized IgG4 monoclonal antibody, that mimics the function of FVIIIa. Its subcutaneous administration is effective and safe in preventing bleeding in patients with severe hemophilia A with or without inhibitor. Although emicizumab has been approved with an administration regimen based on body weight and without monitoring of plasma levels, emicizumab plasma quantification may be useful in different clinical and research circumstances. Since emicizumab-specific commercial calibrators and controls are not yet available in Argentina, we have validated a modified one-stage FVIII assay (modOSA) for the quantification of emicizumab in plasma (Epq) using in-house prepared calibrators and controls. Materials and methods: For Epq a 1/80 sample predilution with Owren Koller buffer was used. In house emicizumab calibrator (150 μg/mL emicizumab) was prepared by adding emicizumab 150 mg/mL to FVIII deficient plasma. Two in house control levels and a 6-point calibration curve were prepared. The validation procedures were performed in a STA Compact Max2 analyser (Diagnostica Stago): Repeatability; controls were processed 20 times in the same analytical run, Intra-laboratory Imprecision; controls were processed in triplicate for 5 days, Linearity; 11 levels were measured in triplicate, Limit of quantitation; 15 measurements of a commercial FVIII deficient plasma were assessed, Bias were estimated based on an external quality assessment program (UK NEQAS). The interference of FVIII and rFVIIa in Epq and of emicizumab in other hemostasis determinations were evaluated. Results: Epq showed acceptable imprecision and bias, a linear range of 5-150 µg/ml and a quantification limit of 5 µg/ml.
Epq was interfered with FVIII but not with rFVIIa. Emicizumab shortened aPTT values below the lower limit of the local reference interval. FVIII measured by chromogenic method with components of bovine origin was not affected. The one-stage FVIII assay (OSA) was falsely increased but showed a strong linear correlation with Epq in this instrument reagent system. Discussion: The automated “in-house” modOSA allows the plasma quantification of emicizumab using a simple, reproducible, low-cost method that is easy to integrate into routine processes.Introducción:
El emicizumab (EMI, Hemlibra®, ROCHE) es un anticuerpo monoclonal IgG4 bi-específico, recombinante y humanizado, con afinidad por el FIXa y el FX, mimetizando la función del FVIIIa. Su administración por vía subcutánea es eficaz y segura en la prevención de hemorragias en pacientes con hemofilia A severa (HAS) con o sin inhibidor. El emicizumab ha sido aprobado con un régimen de administración basado en el peso corporal (1.5 mg/kg por semana, 3 mg/kg cada 2 semanas, 6 mg/kg cada 4 semanas). La cuantificación plasmática de emicizumab podría ser de utilidad en distintas circunstancias clínicas y de investigación: para personalizar el régimen de dosificación optimizando el uso de los viales disponibles y permitiendo una dosificación más costo-efectiva, para valorar la adherencia al tratamiento, ante la sospecha del desarrollo de anticuerpos anti-emicizumab y con fines de investigación(1). Recientemente, una revisión sistemática demostró una relación lineal dosis-concentración y una variabilidad interindividual moderada en la concentración plasmática de emicizumab(2). En esta revisión, la tasa anual de sangrado no mejoró a concentraciones de emicizumab por encima de 25-30 μg/mL, lo que podría permitir una dosificación más baja en una proporción sustancial de pacientes con Hemofilia A (HA). Estos autores proponen un tratamiento basado en una adecuación de la dosis por peso corporal ajustado con la cuantificación plasmática de emicizumab, permitiendo una dosificación más costo-efectiva. En otra publicación, los mismos autores, a fin de evitar desechar la medicación, proponen utilizar viales completos basados en que existe una relación lineal entre los 3 regímenes de tratamiento propuestos en los ensayos clínicos; con lo cual la utilización de dosis alternativas daría lugar a concentraciones plasmáticas similares, con igual efectividad para el control del sangrado(3). Además, esto podría implicar una menor frecuencia de inyecciones como un beneficio adicional, especialmente en niños.
La concentración plasmática de emicizumab puede ser monitoreada mediante modificaciones del ensayo coagulométrico en una etapa para FVIII, utilizando una alta pre-dilución de la muestra, calibradores y controles específicos de emicizumab(4). Debido a que en Argentina aún no están disponibles los calibradores y controles comerciales específicos de emicizumab, hemos validado un método de FVIII coagulométrico de una etapa modificado (modFVIIIcoag) para la cuantificación plasmática de emicizumab (Epc) utilizando calibradores y controles preparados“in-house” (5).
Materiales y Métodos:
Reactivosymateriales utilizados:
• Kit STA®-C.K. Prest®, Diagnostica Stago S.A.S:
ü Reactivo 1: liofilizado de cefalina (sustituto de plaquetas), preparado a partir de tejido de cerebro de conejo.
ü Reactivo2: suspensión tamponada de caolín (5mg/ml) presentado en vial de 5ml.
• Plasma deficiente en FVIII: STA®-ImmunoDef VIII, Diagnostica Stago S.A.S. Reactivo liofilizado.
Los reactivos se reconstituyen acorde a las especificaciones del fabricante.
• STA®-CaCl2 0,025M, Diagnostica Stago S.A.S. Listo para usar.
• STA®-Buffer de Owren-Koller (bOK), Diagnostica Stago S.A.S. Listo para usar.
• Calibrador “in-house” CALEMI: para su preparación se realizan dos diluciones secuenciales (1/100 + 1/10) de emicizumab 150 mg/ml en plasma deficiente en FVIII para alcanzar una dilución final 1/1000. Este material se prepara cada vez que se realiza una curva de calibración.
• Controles de calidad interno “in-house”: nivel 1 = 25 μg/mL de emicizumab (dilución 1/6 de CALEMI en plasma deficiente en FVIII), nivel 2 = 75 μg/mL de emicizumab (dilución 1/2 de CALEMI en plasma deficiente en FVIII). Deben prepararse y utilizarse dentro de las 4h.
• TTPa: STA-PTT Automate, Diagnostica Stago, S.A.S. France.
• FVIII coagulométrico en una etapa (FVIIIcoag): STA®-C.K.Prest®, STA®-ImmunoDef VIII.
• FVIII cromogénico con componentes de origen bovino (FVIIIcro): Coamatic® FVIII Chromogenix, Instrumentation Laboratory Company, USA.
ü S-2765 + I-2581: sustrato cromogénico (N-a-Z-D-Arg-Gly-Arg-pNA) (7.7mg), e inhibidor sintético de trombina (0.2mg) con manitol (agente de volumen).
ü Factor Reagent: Factor IXa bovino (0.3U), Factor X (2.7UI) y trombina (1 NH-U) coliofilizado con CaCl2 (40mmol) y fosfolípidos (0.2mmol).
ü Buffer Tris concentrado que contiene NaCl y BSA. Se diluye 1/10 en agua destilada (Tris 0.025 M, PH 7.9, 1% BSA).
• Coagulómetro automático STA Compact Max2, Diagnostica Stago, S.A.S. France.
Cuantificación plasmática de emicizumab:
El método está basado en el ensayo automatizado de FVIII
coagulométrico en una etapa modificado. Se utiliza una alta pre-dilución de la
muestra (1/80 en bOK) realizada automáticamente por el STA Compact Max2. Para
realizar la curva de calibración en un rango de 5 a 150 μg/mL de emicizumab se utiliza
el calibrador “in-house” CALEMI, del cual se requieren altas diluciones que
no son posibles de realizar de manera automatizada en el STA Compact Max2. Por
lo tanto, es necesario preparar en forma manual una predilución 1/80 del
calibrador con bOK y luego el coagulómetro realiza automáticamente las
siguientes diluciones en bOK: 1:2, 1:4, 1:8, 1:16, 1:32. Para validar cada
calibración se utilizaron los dos niveles de control de calidad interno “in
house”.
Protocolos de validación:
Período de tiempo de validación del método: 3 años.
Curva de Calibración: Consta de 6 niveles de concentración, medidos por duplicado en un Coagulómetro STA Compact Max2, Diagnóstica Stago S.A.S.
Imprecisión: Repetibilidad (CVR); Se procesaron dos niveles de control preparados “in-house” 20 veces en la misma corrida analítica. Imprecisión Intra-Laboratorio (CVIL); se procesaron ambos niveles de control por triplicado durante 5 días, según el protocolo de la guía EP 15-A2 de CLSI(6).
Bias: Se calculó el bias promedio del modFVIIIcoag mediante un programa de evaluación externa de la calidad (UK NEQAS Blood Coagulation, Sheffield UK). Desde el año 2021 al 2023, 8 encuestas fueron procesadas en tiempo real. El bias de cada encuesta fue estimado por la comparación de los resultados obtenidos de nuestro laboratorio con la mediana de los resultados informados por los laboratorios participantes que utilizaron el método de FVIII coagulométrico de una etapa modificado.
Linealidad: Se obtuvieron 11 niveles de concentración de emicizumab utilizando CalEMI (150 μg/mL) y pdFVIII (0 μg/mL) según se muestra en la Tabla 1. A cada nivel se le midió la concentración plasmática de emicizumab por triplicado y se obtuvo el valor medido promedio. Para evaluar la linealidad se utilizó una regresión lineal, calculando la pendiente y la ordenada al origen con un intervalo de confianza del 95%.
Límite de cuantificación (LoQ): Se realizaron 15 determinaciones de Epc en un plasma deficiente en FVIII comercial. Se determinó el LoQ como la concentración igual a 10 veces el desvío estándar (DE) del blanco.
Interferencia del FVIII y del Factor VII recombinante activado (rFVIIa) en la cuantificación plasmática de emicizumab: se prepararon 6 mezclas in vitro de emicizumab con una fuente de FVIII (Unicalibrator. FVIII: 109 UI/dL, Diagnostica Stago S.A.S. France), simulando al plasma de un paciente en tratamiento combinado con emicizumab y concentrado de FVIII. M1 a M5 son mezclas con concentraciones crecientes de emicizumab y decrecientes de FVIII, M3; M6 y M7 tuvieron igual concentración de emicizumab de 50 µg/ml con concentraciones crecientes de FVIII (Tabla 2). A todas las mezclas se les realizó la medición de la concentración plasmática de emicizumab y se les determinó el porcentaje de actividad de FVIII por método cromogénico. Estas mismas determinaciones se realizaron en 7 muestras de descarte de un paciente con HAS con inhibidor anti-FVIII (1,3 UB/ml) que en diferentes situaciones clínicas recibió tratamiento combinado de emicizumab con concentrado de FVIII plasmático (FVIIIp) y rFVIIa.
Interferencias de emicizumab en TTPa, FVIIIcoag y FVIIIcro: se utilizaron las mezclas obtenidas in vitro del ensayo de linealidad (8 de los 11 niveles, en un rango de 5 – 99 μg/mL de emicizumab) y 45 muestras de descarte de 15 pacientes en profilaxis con emicizumab (0.5 a 12.4 años de edad, 11 pacientes con HAS con inhibidor anti-FVIII y 4 pacientes con HAS sin inhibidor). Todas las muestras fueron obtenidas y almacenadas según las recomendaciones internacionales. El TTPa y el FVIIIcoag se realizaron dentro de las 4 horas de la obtención de la muestra, mientras que Epc y el FVIIIcro se analizaron en muestras alicuotadas y almacenadas a -80ºC. Además, se calculó la razón entre FVIIIcoag y Epc (FVIIIcoag/Epc) y la correlación entre ambos.
Aspectos éticos: Para la validación del método los estudios fueron realizados con mezclas in vitro de materiales comerciales y muestras de descarte de pacientes pediátricos con HA. Los padres, madres y/o tutores firmaron un consentimiento informado, aceptando el uso de muestras de descarte para fines de investigación.
Análisis estadístico de los datos: Se utilizó el programa estadístico EP evaluator en la versión 10.0 y el programa Excel versión 2016.
Resultados:
Curva de Calibración: Los resultados medidos en segundos por duplicado en cada curva fueron interpolados con sus respectivos niveles de concentración asignados. Para obtener la ecuación de la curva de calibración se enfrentó log de los segundos en función del log de la concentración. Se obtuvo una ecuación polinomial de segundo orden expresada como: Log(c) = - (a*Log(t)2) + (b*Log(t)) – c (Figura 1).
Se realizaron 8 curvas de calibración a lo largo del protocolo de validación, donde cada curva fue realizada con CALEMI preparado en el momento. En la Tabla 3 se muestran los valores promedios y el desvío estándar (DE) en segundos y el coeficiente de variación porcentual (CV%) entre las distintas curvas de calibración.
Imprecisión: Se obtuvo una Repetibilidad de 4.8% para el nivel 1 y 3.1% para el nivel 2. La imprecisión Intra-Laboratorio para el nivel 1 fue de 5.7% y 4.1% para el nivel 2. Actualmente, no se disponen de requerimientos de calidad en términos de imprecisión aceptable, por tal motivo, hemos comparado nuestros resultados con los reportados por Shinohara S y col(7), encontrando valores similares a los publicados (Tabla 4).
Bias: El bias obtenido del método de FVIII coagulométrico de una etapa modificado fue de 8%. Este valor fue estimado a través del promedio del bias (%) de 7 encuestas de un programa de evaluación externa de calidad (UK NEQAS Blood Coagulation, Sheffield UK). La encuesta 23.02 fue desestimada en el cálculo ya que el nivel de emicizumab era menor al límite de cuantificación. El coeficiente de variación porcentual inter-laboratorio promedio (CV%IL) de las encuestas evaluadas fue de 14.4% (Tabla5). Todos los laboratorios participantes informaron el valor de Epc medido con el método de FVIII coagulométrico de una etapa modificado.
Linealidad: Se obtuvo un rango lineal de 5 a 150 μg/ml de emicizumab, con una correlación entre el valor asignado y el valor medido promedio de 0,9989. La pendiente de la recta fue de 0,9988 y la ordenada al origen de 0,9720 (Figura 2).
Límite de cuantificación: El promedio de las 15 determinaciones del plasma deficiente en FVIII comercial fue de 1,6 µg/ml, con un DE de 0,5 µg/ml, por lo tanto, el límite de cuantificación obtenido fue de 5 µg/ml de emicizumab.
Interferencias: En las mezclas in vitro se encontró una interferencia positiva en la cuantificación plasmática de emicizumab cuando hay presencia de FVIII (Tabla 6, Figura 3). También en las muestras del paciente en tratamiento combinado, la presencia del FVIIIp interfirió positivamente en la determinación de Epc, mientras que el rFVIIa no interfirió (Tabla 7).
Cuando se analizaron las 8 mezclas obtenidas in vitro del ensayo de linealidad, se encontraron los siguientes resultados: a) en el rango de concentración de emicizumab analizado los valores de TTPa siempre estuvieron por debajo del límite inferior del intervalo de referencia, b) la determinación FVIIIcoag fue falsamente afectada por la presencia de emicizumab, mostrando una fuerte correlación con Epc (coeficiente de correlación, r: 0.989), c) una razón promedio FVIIIcoag/Epc de 7 (rango: 6-8), d) el método cromogénico con componentes de origen bovino no se vio interferido por emicizumab (Tabla 8 y Figura 4).
En las muestras de pacientes en régimen de profilaxis con emicizumab se obtuvo un rango de Epc medido de 25 a 88 µg/ml, donde los valores de TTPa también estuvieron por debajo del límite inferior del intervalo de referencia. La determinación FVIIIcoag fue falsamente afectada por la presencia de emicizumab, mostrando un coeficiente de correlación (r) con Epc de 0.8109 y una razón promedio FVIIIcoag/Epc de 8 (rango: 5-12). En estas muestras, la presencia de emicizumab no interfirió en la medición del FVIII cuando se utilizó el método cromogénico con componentes de origen bovino. (Tabla 9 y Figura 5).
Discusión:
El emicizumab es una alternativa terapéutica en pacientes con HA y su cuantificación plasmática podría ser de utilidad para alcanzar un tratamiento personalizado y costo-efectivo(8).
Este es el primer estudio que describe la validación de un método “in house” para la cuantificación plasmática de emicizumab utilizando calibradores y controles preparados en el laboratorio. El método modFVIIIcoag, validado en este sistema reactivo/instrumento, sigue un modelo lineal en un rango amplio de concentración, con una imprecisión comparable a los resultados de la literatura. El Bias fue aceptable, menor al CV% interlaboratorio promedio de las encuestas del programa UK NEQAS mostrando un desempeño comparable al resto de los laboratorios que utilizaron calibradores y controles comerciales (r2 Diagnostics, South Bend, Indiana, United States)”.
La performance analítica de modFVIIIcoag, en este sistema reactivo/instrumento, es similar a la reportada por Donners A y col(9) en la validación del método de Cromatografía líquida/Espectrometría de masa (LC-MS/MS), con la ventaja de que modFVIIIcoag es un método de fácil implementación en los laboratorios y no requiere de un tiempo de 24h para la preparación de la muestra. A diferencia de LC-MS/MS, modFVIIIcoag tiene la limitación de la interferencia por el FVIII que pudiera estar presente en la muestra de los pacientes con tratamiento combinado. Publicaciones recientes proponen la inactivación térmica del FVIII de las muestras (56 °C durante 40 minutos) ó la neutralización de la actividad del FVIII utilizando inhibidores(10).
En las muestras del paciente con HAS, en tratamiento combinado con emicizumab y rFVIIa, se demostró que el agente “bypasseante” no interfiere en el ensayo modFVIIIcoag automatizado “in-house” para la cuantificación plasmática de emicizumab.
En la evaluación de la interferencia por emicizumab en otras determinaciones de hemostasia, observamos, que el TTPa en este sistema reactivo/instrumento se acortó por debajo del límite inferior del intervalo de referencia, debido a que el emicizumab interactúa con FIXa y FX humano y no requiere de una activación previa. Del mismo modo se generó un falso aumento de los niveles medidos de FVIIIcoag, mientras que emicizumab no interfirió en el método FVIIIcro ya que se utilizan componentes de origen bovino.
En las mezclas preparadas in vitro del ensayo de linealidad, el factor estimado a partir de la relación FVIIIcoag/Epc fue en promedio de 7, con un rango de 6 a 8. Sin embargo, en las muestras de pacientes en profilaxis con emicizumab el factor promedio fue de 8, oscilando en un rango amplio de 5 a 12, por lo tanto, esta relación FVIIIcoag/Epc no podría utilizarse como un factor de conversión para estimar la concentración de emicizumab en las muestras de pacientes.
Concluimos que el ensayo modFVIIIcoag automatizado “in-house” permite la cuantificación plasmática de emicizumab mediante un método sencillo, reproducible, de bajo costo y de fácil integración en los procesos de rutina.
Contribución de los autores: Todas las personas autoras han efectuado una contribución sustancial a la concepción o el diseño del estudio o a la recolección, análisis o interpretación de los datos; han participado en la redacción del artículo o en la revisión crítica de su contenido intelectual; han aprobado la versión final del manuscrito; y son capaces de responder respecto de todos los aspectos del manuscrito de cara a asegurar que las cuestiones relacionadas con la veracidad o integridad de todos sus contenidos han sido adecuadamente investigadas y resueltas.
Bibliografía
1. Tripodi A, Chantarangkul V, Novembrino C y col. Emicizumab, the factor VIII mimetic bi-specific monoclonal antibody and its measurement in plasma. Clin Chem Lab Med. 2020;59:365-371.
2. Donners AAMT, Rademaker CMA, Bevers LAH y col. Pharmacokinetics and Associated Efficacy of Emicizumab in Humans: A Systematic Review. Clin Pharmacokinet. 2021;60:1395-1406.
3. Donners AAMT, van der Zwet K, Rademaker CMA, Egberts TCG, Schutgens REG, Fischer K. The efficacy of the entire-vial dosing of emicizumab: Real-world evidence on plasma concentrations, bleeds, and drug waste. Res Pract Thromb Haemost. 2023;7:1-9.
4. Müller J, Pekrul I, Pötzsch B, Berning B, Oldenburg J, Spannagl M. Laboratory Monitoring in Emicizumab-Treated Persons with Hemophilia A. Thromb Haemost. 2019;119:1384-1393.
5. Sueldo E, Annetta E, Frontroth J, Hepner M. Cuantificación plasmática de emicizumab. Revista Hematología, 2022; 26, 96–98.
6. CLSI. User Verification of Performance for Precision and Trueness; Approved Guideline—Second Edition. CLSI document EP15-A2. Wayne, PA: Clinical and Laboratory Standards Institute; 2005.
7. Shinohara S, Saito T, Noguchi-Sasaki M, Ishiwata T, Morris M. Evaluation of Emicizumab Calibrator and Controls with a Modified One-stage FVIII Assay on an Automated Coagulation Analyzer. ISTH Academy; Laboratory Diagnostics – Bleeding. 2019: PB1305.
8. Bukkems LH, Fischer K, Kremer-Hovinga I y col. Emicizumab Dosing in Children and Adults with Hemophilia A: Simulating a User-Friendly and Cost-Efficient Regimen. Thromb Haemost. 2022;122:208-215.
9. Donners AAMT, Gerencsér L, van der Elst KCM y col. Quantification of emicizumab by mass spectrometry in plasma of people with hemophilia A: A method validation study. Res Pract Thromb Haemost. 2022;6:e12725.
10. Hamedani NS, Donners AAMT, van Luin M y col. Functional determination of emicizumab in presence of factor VIII activity. J Thromb Haemost. 2023;21:3490-3500.
Tablas
Tabla 1. Ensayo de linealidad. Mezclas in vitro de Calibrador “in-house”(CALEMI) y plasma deficiente en FVIII (pdFVIII)
|
Valor Asignado µg/ml |
CALEMI (µl) |
pdFVIII (µl) |
|
150 |
500 |
0 |
|
99 |
330 |
170 |
|
75 |
250 |
250 |
|
51 |
170 |
330 |
|
39 |
130 |
370 |
|
30 |
100 |
400 |
|
21 |
70 |
430 |
|
9 |
30 |
470 |
|
5 |
15 |
485 |
|
3 |
10 |
490 |
|
0 |
0 |
500 |
|
Tabla 2. Ensayo de interferencia. Mezclas in vitro de emicizumab y Unicalibrator |
|
Mezclas |
Volumen (µl) de Emicizumab de 100 µg/ml |
Emicizumab Valor asignado (µg/ml) |
Volumen (µl) de Unicalibrator de 109 UI/dL |
FVIII Valor asignado (UI/dL) |
|
M1 |
0 |
0 |
500 |
109 |
|
M2 |
125 |
25 |
375 |
82 |
|
M3 |
250 |
50 |
250 |
55 |
|
M4 |
375 |
75 |
125 |
27 |
|
M5 |
500 |
100 |
0 |
0 |
|
M6 |
200 |
50 |
200 µl de Unicalibrator al ½ (55 UI/dL) |
27 |
|
M7 |
10 µl de Emicizumab 1500 µg/ml |
50 |
290 |
105 |
Tabla 3. Resultados de 8 Curvas de calibración del método modFVIIIcoag para la cuantificación plasmática de emicizumab (Epc).
|
Epc asignado (µg/ml) |
Promedio (seg) |
DE (seg) |
CV% |
|
150 |
45,1 |
1,5 |
3,3 |
|
75 |
51,2 |
1,6 |
3,1 |
|
38 |
58,3 |
1,6 |
2,8 |
|
19 |
66,0 |
1,7 |
2,5 |
|
9 |
73,1 |
1,6 |
2,1 |
|
5 |
79,5 |
1,1 |
1,4 |
|
Nivel 1 |
Nivel 2 |
Literatura, Level 1 |
Literatura, Level 2 |
||||||||
|
Epc (µg/ml) |
CVR (%) |
CVIL (%) |
Epc (µg/ml) |
CVR (%) |
CVIL (%) |
Epc (µg/ml) |
CVR (%) |
CVIL (%) |
Epc (µg/ml) |
CVR (%) |
CVIL (%) |
|
26,0 |
4,8 |
5,7 |
74,0 |
3,1 |
4,1 |
26,2 |
4,7 |
4,7 |
75,0 |
2,6 |
3,3 |
|
|
Encuesta 21:01 |
Encuesta 22:01 |
Encuesta 22:02 |
Encuesta 22:03 |
|
Epc medido (µg/ml) Bias (%) Mediana(IL) (µg/ml) (rango)
CV%(IL) N laboratorios |
57,4 -3,45 59,5 (50,4 – 68,0)
8,8 30 |
42,7 5,20 40,6 (25,3 – 56,0)
15,2 31 |
71,0 0,28 70,8 (58,3 – 90,4)
10,3 31 |
20,8 -0,95 21,0 (16,8 – 24,1)
6,3 33 |
|
|
Encuesta 22:04 |
Encuesta 23:01 |
Encuesta 23:02 |
Encuesta 23:03 |
|
Epc medido (µg/ml) Bias (%) Mediana(IL) (µg/ml) (rango)
CV%(IL) N laboratorios |
16,8 34,40 12,5 (0,3 – 20,8)
39,8 32 |
64,1 -0,08 64,4 (53,7 – 77,8)
9,6 37 |
1,1 *** 0,2 (0,0 – <10,0)
151,8 37 |
55,1 -12,00 62,6
11,0 34 |
Tabla 5. Estimación del Bias. Resultados de 8 encuestas de un control de calidad externo.
|
Mezclas |
Emicizumab Valor teórico (µg/ml) |
EmicizumabValor medido (µg/ml) |
FVIII Valor teórico (UI/dl) |
FVIIIcro Valor medido (UI/dl) |
|
1 |
0 |
25 |
109 |
113 |
|
2 |
25 |
48 |
82 |
90 |
|
3 |
50 |
66 |
55 |
53 |
|
4 |
75 |
83 |
27 |
30 |
|
5 |
100 |
98 |
0 |
<1 |
|
6 |
50 |
57 |
27 |
28 |
|
7 |
50 |
77 |
105 |
106 |
Tabla 6. Resultados del ensayo de interferencia en mezclas in-vitro de emicizumab y Unicalibrator.
|
Muestras/Tratamiento
|
Epc (µg/ml) |
FVIIIcro (UI/dl) |
|
1/ Profilaxis con Emicizumab (Fase mantenimiento) |
61 |
<1 |
|
2/ Emicizumab + FVIII 100U/kg, 1h post infusión |
82 |
92 |
|
3/ Emicizumab + FVIII 100U/kg, 9h post infusión |
75 |
45 |
|
4/ Emicizumab + FVIII 100U/kg, 12h post infusión |
63 |
12 |
|
5/ Emicizumab + FVIII 100U/kg, 1.5h post infusión |
80 |
74 |
|
6/ Emicizumab + FVIII 100U/kg, 0.5h post infusión |
60 |
9 (Nivel de FVIII menor al esperado) |
|
7/ Emicizumab + rFVIIa, 0.5h post infusión |
58 |
<1 |
|
8/ Emicizumab + rFVIIa, 0.2h post infusión |
58 |
<1 |
|
Tabla 7. Resultados de un paciente en tratamiento combinado de emicizumab con concentrado de FVIII plasmático (FVIIIp) y Factor VII recombinante activado (rFVIIa). Epc: cuantificación plasmática de emicizumab. FVIIIcro: FVIII por método cromogénico con componentes de origen bovino. |
|
Tabla 8. Interferencias de Emicizumab en otras determinaciones de hemostasia evaluadas en mezclas in vitro |
|
TTPa (34,0-42,0 seg) |
Valor Promedio Epc (µg/ml) |
FVIIIcoag (UI/dl) |
FVIIIcoag/Epc |
FVIIIcro (UI/dl) |
|
24,0 |
100 |
650 |
7 |
<1 |
|
24,7 |
77 |
480 |
6 |
<1 |
|
25,4 |
52 |
360 |
7 |
<1 |
|
25,5 |
40 |
300 |
8 |
<1 |
|
26,2 |
31 |
230 |
7 |
<1 |
|
26,9 |
22 |
143 |
7 |
<1 |
|
29,8 |
10 |
77 |
8 |
<1 |
|
31,9 |
5 |
35 |
7 |
<1 |
|
Muestras de pacientes en profilaxis con emicizumab |
|||||
|
n = 45
|
TTPa (seg) |
Epc (µg/ml) |
FVIIIcoag (UI/dl) |
FVIIIcoag/Epc |
FVIIIcro (UI/dl)
|
|
Promedio |
29,0 |
49 |
392 |
8 |
<1 |
|
Min |
24,0 |
25 |
187 |
5 |
<1 |
|
Max |
34,0 |
88 |
660 |
12 |
<1 |
|
Tabla 9. Resultados de las muestras de pacientes en profilaxis con emicizumab Epc: cuantificación plasmática de emicizumab FVIIIcro: Actividad de FVIII por método cromogénico FVIIIcoag: Actividad de FVIII por método coagulométrico en una etapa
|
Figuras
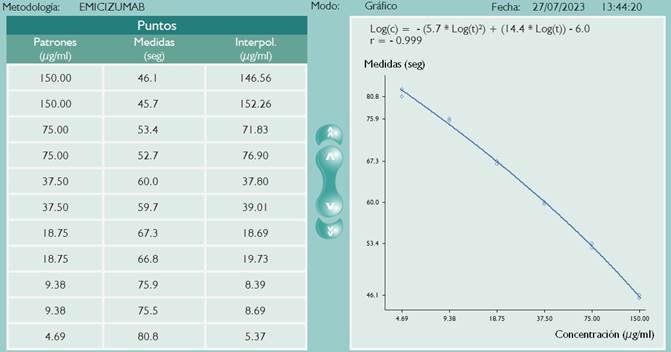
Figura 1. Curva de calibración de modFVIIIcoag para la cuantificación plasmática de emicizumab

Figura 2. Resultados del ensayo de linealidad
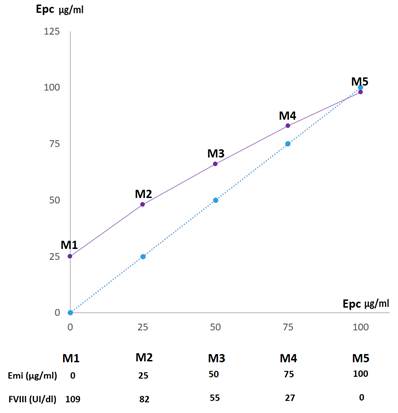
Figura 3. Resultados del ensayo de interferencia del FVIII en Epc. La línea punteada de color celeste representa el valor esperable de Epc en las mezclas. La línea de color violeta grafica la concentración plasmática de emicizumab medida (Epc, µg/ml) en las mezclas con concentraciones decrecientes de FVIII y concentraciones crecientes de emicizumab.
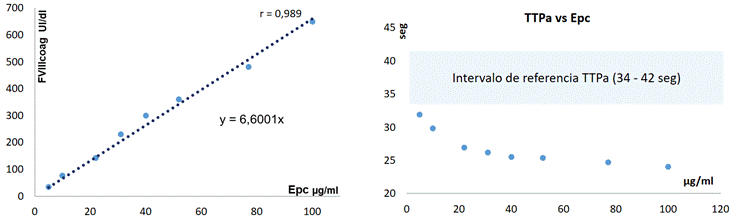
Figura 4. Interferencias de emicizumab en otras determinaciones de hemostasia evaluadas en mezclas in vitro: Tiempo de tromboplastina parcial activado (TTPa). Actividad de FVIII coagulométrico en una etapa (FVIIIcoag).
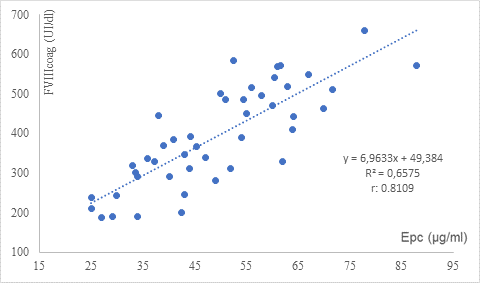
Figura 5. Resultados de FVIII caogulométrico en una etapa (FVIIIcoag) vs la cuantificación plasmática de emicizumab (Epc) en muestras de pacientes en profilaxis con emicizumab.